აირჩიეთ მკითხველი
პოპულარული სტატისტიკა
თუ ზედაპირზე დაასხით ნატურალური წყლის წვეთი და შეიზილეთ აორთქლებამდე, მაშინ წვეთების ადგილზე თეთრი გამოყოფა გამოჩნდება - და წყალში მარილები კრისტალიზდება. ბუნებრივ წყლებში მარილების არსებობა ათასობითჯერ იზრდება. მაგალითად, ლიტრი წვიმის წყალი შეიცავს ერთ ან მეტ ათეულ მილიგრამს მარილს. ხოლო ყარა-ბოგაზ-გოლის შესასვლელიდან (კასპიის ზღვა) ლიტრ წყალში - 300 გ, შესაძლოა მასის მესამედი.
წყლის გამოყენებაში მეტი მარილი მნიშვნელოვანია, როგორც იონები. ბუნებრივ წყლებში სამი ანიონი მნიშვნელოვანია ( ჰიდროკარბონატი HCO 3 -, ქლორიდი Cl -і სულფატი SO 4 2-) და რამდენიმე კატიონი ( კალციუმი Ca 2+, მაგნიუმი მგ 2+, ნატრიუმის Na+і კალიუმი K+) - მათ თავის იონებს უწოდებენ. ქლორიდის იონები წყალს მარილიან გემოს მატებს, სულფატის იონები, კალციუმის და მაგნიუმის იონები მწარეა, ჰიდროკარბონატული იონები არ არის ქონდარი. მტკნარ წყლებში სუნი აღემატება 90-95%-ს, ხოლო მაღალმინერალიზებულ წყლებში - ყველა მდინარის 99%-ზე მეტს. ძირითადი იონების კონცენტრაციის ქვედა ზღვარი არის 1 მგ/ლ, ამიტომ ზოგიერთ შემთხვევაში, მაგალითად, ზღვის და ზოგიერთი მიწისქვეშა წყლებისთვის, ძირითად კომპონენტებს ასევე შეიძლება დაემატოს Br -, B 3+, Sr 3+ და ა.შ. K + იონების დამატება თავთა და უკანა რაოდენობაზე. მიწისქვეშა და ზედაპირულ წყლებში ეს იონები, როგორც წესი, განსხვავებულ პოზიციას იკავებენ. მხოლოდ K+ იონებს ატმოსფერულ ვარდნაში შეუძლიათ მნიშვნელოვანი როლი შეასრულონ.
დენის ძირითადი კომპონენტების პროტეიონული ფორმა ყოველთვის სასარგებლოა დაბალმინერალიზებული წყლებისთვის. როდესაც იონებს შორის კონცენტრაცია იზრდება, მაშინ იქნება ურთიერთქმედება, პირდაპირი ასოციაცია. პროცესი, საპირისპირო დისოციაცია. ამ შემთხვევაში იქმნება ასოცირებული იონური წყვილი, მაგალითად MgHCO 3 + CaHCO 3 +.
კლიმატური და სხვა გონების შემოდინებით, ბუნებრივი წყლების ქიმიური შენახვა იცვლება და წარმოქმნის დამახასიათებელ ნიმუშებს, ზოგიერთი სპეციფიკური ბუნებრივი წყლების სხვადასხვა ტიპებისთვის (ატმოსფერული ჩავარდნა, მდინარეები, ტბები, მიწისქვეშა წყლები).
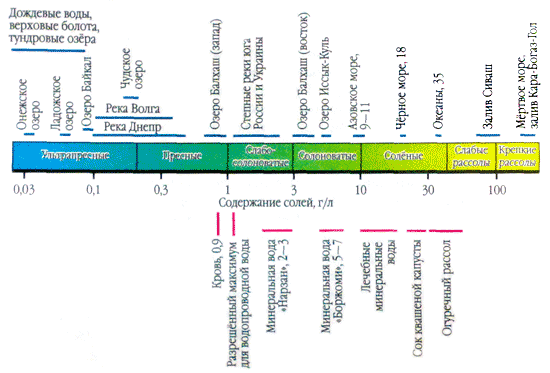
ატმოსფერული ვარდნაყველა ბუნებრივი წყალი ყველაზე ნაკლებად მინერალიზებულია, მაგრამ მათი ნივთიერებების ქიმიური შენახვის მიღმა, სუნი არანაკლებ მრავალფეროვანია, ვიდრე სხვა ბუნებრივი წყლები. ჯერელომის საწყობი არის ატმოსფეროს აეროზოლები. საწყობი არის სხვადასხვა სახის. როდესაც რუსეთის ევროპულ ნაწილში ატმოსფერული ჩამონადენის საშუალო მდიდარი მინერალიზაციაა 10-20 მგ/ლ დიაპაზონში და ექსტრემალური მნიშვნელობები მთელი ტერიტორიისთვის 3-4 და 50-60 მგ/ლ იონი, ეს საწყობი ხასიათდება. სიმკაცრით და შუა ანიონები ყველაზე მნიშვნელოვანია SO 4 2- ან HCO 3 - , ხოლო კათიონების შუა ნაწილი ინახება დისტანციურ დონეზე, რათა დაზოგოს Ca 2+ ან Na +. ზღვიდან ქარის თავიდან აცილების მიზნით, ქარის მიერ მარილების მექანიკური მოცილების გამო, ნარჩენებში იზრდება ქლორის კონცენტრაცია. კონსერვაციის შედეგად, Cl-ის წყლის კონცენტრაცია ეცემა და SO 4 2-, Ca 2+ და Mg 2+, თუმცა, მაღლა მოძრაობს. SO 4 2- და Ca 2+-ის ნაცვლად მოძრაობის მიზეზი არის ატმოსფეროს გამდიდრება კონტინენტური მოძრაობის აეროზოლებით. როდესაც სამყარო კონტინენტზე ღრმად მიდის, ზღვის აეროზოლების ნაწილი ირეცხება. SO 4 2--ის კონცენტრაცია აჩვენებს უდიდეს ცვლილებებს. თუ Ca 2+ და Na + დამატება მიბმულია ნიადაგებისა და ფორების მინერალური ხერხით, რომლის ზედაპირზე ყოველთვის არის მარილი, მაშინ ერთ მხარეს მოთავსებულია SO 4 2 დამატება, SO 2 დაჟანგვა და. H 2 S, წინააღმდეგ შემთხვევაში - მარილიანი ზედაპირებიდან მჟავე მარილების აწევა.
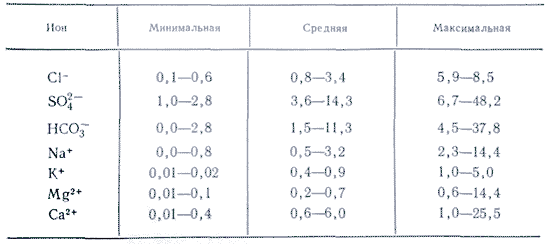
შეუძლებელია შეაფასოს მარილის ნაწილაკების დიდი რაოდენობა, რომლებიც ამოდის ნიადაგიდან, მარილის ტბებიდან, ყინულის ზედაპირზე, განაყოფიერებისა და ფოთლოვანი ნივთიერებების, რომლებიც გამოიყოფა ქიმიურ და მეტალურგიულ ნივთიერებებად. ისინი გამოიყოფა ატმოსფეროში სხვა ზემოქმედების შედეგად. ადამიანის მოქმედებები და შემდეგ ჩამოირეცხება ნალექით.
მორწყეთ მდინარის უმეტესი ნაწილიდაწექით ჰიდროკარბონატების კლასამდე. კათიონების შენახვის მიღმა ეს წყალი შესაძლოა კალციუმსაც შეიცავდეს; ჰიდროკარბონატული წყლები მაგნიუმის და ნატრიუმის მაღალი კონცენტრაციითაც კი იშვიათია. ჰიდროკარბონატული კლასის ბუნებრივ წყლებს აქვთ ყველაზე მეტი წყალი დაბალი მინერალიზაციით (მარილების საერთო შემცველობა 200 მგ/ლ-მდე).
მდინარეები წყლით, რომელიც აღწევს სულფატის კლასს, თითქმის უთვალავია. სუნი უფრო ფართოა, განსაკუთრებით სტეპის სმუზიებში და ხშირად ცარიელებში. სულფატური კლასის ბუნებრივ წყლებში კათიონების შენახვაში, ისევე როგორც ჰიდროკარბონატული კლასის წყლებში, ჭარბობს კალციუმი. თუმცა, სულფატების კლასის მდინარეებს ჭარბი წონა აქვთ ნატრიუმით. სულფატური კლასის წყლის მინერალიზაციის მიხედვით მნიშვნელოვანია ჰიდროკარბონატული კლასის წყლის გადაჭარბება. მდინარის სულფატური წყლები დაბალი (მყარი შემცველობა 200 მგ/ლ-მდე) და საშუალო (მყარი შემცველობა 200-დან 500 მგ/ლ-მდე) მინერალიზაციით იშვიათად იზრდება თანაბრად. ამ მდინარისთვის ყველაზე დამახასიათებელია მისი დაბალი (მარილის შემცველობა 500-დან 1000 მგ/ლ-მდე), რაც მაღალია (მარილის შემცველობა 1000 მგ/ლ-ზე მეტი) წყლის მინერალიზაცია.
მდინარეები, რომელთა წყლები ქლორიდის დონეს აღწევს, ისეთივე იშვიათად წარმოიქმნება, როგორც მდინარეები, რომელთა წყლები შეიცავს სულფატებს. ამ ტერიტორიის წინ არის ყველაზე მნიშვნელოვანი სტეპური რაიონები, მაგრამ ამაოდ. ბუნებრივი წყლების ყველაზე მნიშვნელოვანი კათიონები არის ქლორიდის კლასი, ძირითადად ნატრიუმი. ქლორიდის კლასის წყლებს აქვთ მაღალი მინერალიზაცია - 1000 მგ/ლ-ზე მეტი, 500-დან 1000 მგ/ლ-მდე.
მდინარის წყლის იონური შენახვის მახასიათებლები ტარდება ზაფხულის პერიოდამდე. სასიმღერო სამყარომდე ის ახასიათებს საწყობს და ყინულის ვარდნის საათს. ეს ნიშნავს, რომ გაზაფხულის სეზონზე ნაკლებად წყლის მინერალიზაციაა აცილებული.
რუსეთში მდინარის წყლის იონური შენახვის განაწილების თანმიმდევრული ნიმუში არსებობს. არსებობს ზოგადი ტენდენცია წყლის მინერალიზაციის გაზრდისკენ რუსეთის ევროპული ნაწილის უფრო დიდ ტერიტორიაზე ყოველდღიურად და დაღმართის დასაწყისიდან. მდინარის წყლების იონური შენახვის ზონალობა აიხსნება ახლანდელი დროის კლიმატის შეგნებული გონების მოქმედებით და წარსულის კლიმატით. ნიადაგებისა და ქანების ტენიანობის დონე, მათში ადვილად აქროლადი მარილების არსებობა და ნიადაგების მარილიანობა სხვადასხვა კლიმატური გონების მდიდარი შემოდინების ბუნებრივი შედეგია. გაანადგურეთ რუსეთის მდინარის წყლის ქიმიური საწყობის ზონალობა და მათი დაბინძურების სახეობებისა და გონების საწყობის მნიშვნელობა.


ტბის წყლის მინერალიზაცია და ქიმიური შენახვაცვლილება მდინარიდან მდინარეში იცვლება ძალიან ფართო საზღვრებში. მდინარეები, რომელთა წყლის მინერალიზაცია 100-200 მგ/ლ-ზე მეტია, რატომღაც იყო სუნი, იშვიათი მოვლენაა, ტბის წყლის მინერალიზაცია კი დაბალია, რამდენიმე ათეული მგ/ლ (სულ მცირე აწევა ფიცრიდან) ძალიან. მაღალი 3 -3,5% (მარილის ტბები ვარდის მარილწყალთან ერთად კიდემდე მარილებით გაჟღენთილი). მინერალიზაციის შემცველობაზე გავლენას ახდენს ტბის წყლის იონური შენახვა. არავინ იცის მდინარის წყლის კანონების, სიმძლავრის და ქიმიური შენახვის შესახებ. ტბის წყლის გაზრდილი მინერალიზაციით, მის შენახვაში იონების სწრაფი ზრდა ხდება შემდეგი თანმიმდევრობით: HCO 3 - →SO 4 2- →Cl -; Ca 2+ →Mg 2+ →Na + . როდესაც მინერალიზაცია ტბის წყალში 500-1000 მგ/ლ აღწევს, ჭარბობს ჰიდროკარბონატული იონები, 0,1%-ზე მეტი - ყველაზე ხშირად სულფატური, ხოლო 0,3-0,5%-ის მიღწევის შემდეგ, წყლის ლითოლოგიური მახასიათებლების მიხედვით.მტკნარი წყალი - სულფატი ან ქლორიდი. . ტბის წყლებში კათიონების შენახვაში მნიშვნელოვანია კალციუმის როლი, დაზოგულია 0,1-0,2%-ზე ნაკლები. მინერალიზაციის შემდგომი ზრდასთან ერთად, ნატრიუმი იწყებს ამ როლის შესრულებას. ისინი ინარჩუნებენ მაგნიუმს, ისევე როგორც ყველა სხვა წყალს, შუალედურ მდგომარეობაში ყველა მინერალიზაციის დროს. იონური შემადგენლობის ამ დაყოფის მიზეზი მდგომარეობს სხვადასხვა სახის მარილებში. სუფთა ტბების ყველაზე მნიშვნელოვანი ნაწილი, როგორიცაა მდინარეები, ჰიდროკარბონატულ-კალციუმიანი წყლების შენახვის უკან.
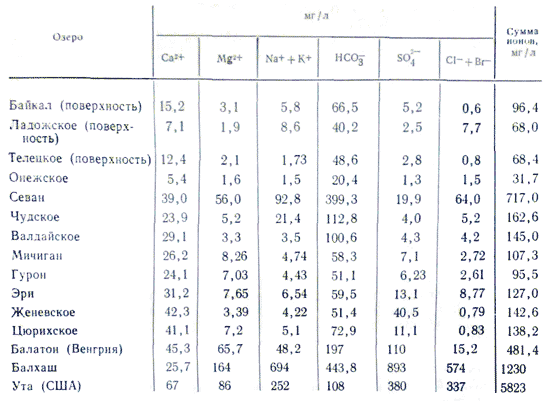
მარაგი ზღვის წყალი ახასიათებს დიდი რაოდენობით მარილები. კონტინენტურ წყლებში ყველაზე ხშირად შეინიშნება შემდეგი კონცენტრაციის კოეფიციენტები: HCO 3 - > SO 4 2- > Cl - და Ca 2+ > Mg 2+ > Na + ან Ca 2+ > Na + > Mg 2+, შემდეგ მლაშე და ზღვის წყლები, დაწყებული ჰალალის მინერალიზაციიდან 1 გ/კგ, თანაფარდობა იცვლება: Cl - > SO 4 2- > HCO 3 - და Na + > Mg 2+ > Ca 2+. მდინარიდან ზღვის წყლამდე წყლებს შორის ურთიერთობის ცვლილება აიხსნება ბოლოდროინდელი მიღწევებით დაბალი ხარისხის მარილების მნიშვნელობით წყლის გაზრდილი მინერალიზაციის სამყაროში. საერთო ჯამში, ისინი და ძირითადი კომპონენტების ნახევარი შეადგენს ოკეანის წყლისა და მინერალური ნაკადების ყველა კომპონენტის 99,99%-ს.
ოკეანის წყლის ძირითადი მარილის საწყობის ელემენტებს შორის, კანსა და მათ ჯამს შორის, არის პრაქტიკული ფოლადი კონცენტრაციასთან მიმართებაში. დარჩენილი yogo dov U. Ditmar, vykonav ახალი ქიმიური ანალიზი (ქლორიდები, სულფატები, კალციუმი, მაგნიუმი, ნატრიუმი) 77 წყლის ნიმუშები მიწოდებული ყველა ოკეანედან ექსპედიციის სხვადასხვა სიღრმეებიდან "ჩელენჯერზე": წყალში ღია ოკეანეში განურჩევლად ნახშირორჟანგის აბსოლუტური კონცენტრაცია მარილის ძირითადი საწყობის ძირითად კომპონენტებს შორის ყოველთვის მუდმივია (დიტმარის კანონი). PID ერთად Viparovvannya Vyparovvannya, სიწყნარე, მოსაწყენი tannna lodiv შაბათი ტილები მარილები, ძირი marshmallow, ale -ahled Morskiye, საზღვარგარეთ in intergles არ არის უკიდეგანო უზარმაზარობა არ გველის. ასეთი წოდება, yakshcho vіdomo, არის კილკოსტის აზოტის მარილების I კონცენტრატების დრო, 1 კგ წყლის ძირითადი კომპონენტები იმავე ინგრედის კონცენტრატებამდე, ლიქენი ერთ-ერთი ღვთისმსახურებისთვის შეუძლია გამოთვალოს ხსნის საწყობი. ოკეანის დრაივი. ასეთი "საცნობარო" ინგრედიენტის კონტექსტში არის "ქლორიანობა", რომელიც არის რამდენიმე გრამი ქლორის იონები, რაც ექვივალენტურია ჰალოგენების (მათ შორის, ფტორიდები, რომლებიც არ არის ნალექი ნიტრატით) 1 კგ ზღვის წყალში. (სორენსენს დაევალა). ოკეანის წყლის საწყობის სტაბილურობა ადვილად ანადგურებს კონტინენტური ჩამონადენის შემოდინებით, რომელიც განახლდება, ესტუარულ რაიონებში და შიდა ზღვების მახლობლად, ოკეანესთან რთული წყლის გაცვლით. ძირითადი კომპონენტების საწყობში კალციუმის და მაგნიუმის კათიონების კონცენტრაცია, ასევე სუსტი მჟავების ანიონების კონცენტრაციის ჯამი (HCO 3 -, CO 3 2-, H 2 BO 3 -) მნიშვნელოვნად დაბალია 1-ით. % სპ-ის სტაბილიზაციაში დამატებულია კავშირში დერივატიზებულ კარბონატ კალციუმთან წყლის ზედაპირულ ბურთულებში და წყლის დაშლა თიხაზე.
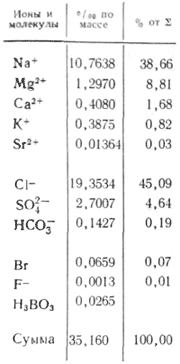
მიკროელემენტების კონცენტრაცია ტაბლეტში მცირეა, ასე რომ, სუნის რაოდენობა აღემატება ყველა გახსნილი მარილის წონით 0,01%-ს. უკანა ხაზის სიგნალიზაცია V.V. გორდევა და ა.პ. მიკვლეულია ლიზიცინი, რომელშიც ყველაზე მაღალი კონცენტრაციაა ლითიუმი (180 მკგ/ლ), რუბიდიუმი (120 მკგ/ლ), ბარიუმი (18 მკგ/ლ), ყველაზე დაბალი - ოქრო (0,004 მკგ/ლ), იშვიათი მიწის ელემენტები (ნაკლები). ვიდრე 0,001 მკგ ლ) რადიუმი (10 -7 მკგ/ლ).
რაც უფრო იზოლირებულია ზღვა ოკეანედან, მით უფრო განსხვავდება მისი წყლის შენახვა ოკეანეში წყლის შენახვისგან. უპირველესი მნიშვნელობისაა ოკეანესთან წყლის გაცვლა, კავშირი კონტინენტური ჩამონადენისა და ზღვის მოცულობას შორის, ზღვის სიღრმე და მასში ჩაედინება მდინარეში წყლის ქიმიური შენახვის ბუნება.
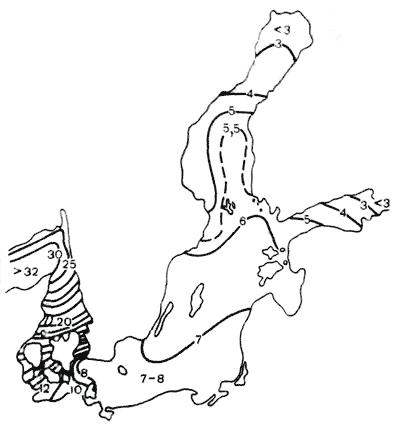
მიწისქვეშა წყლებიმათ აწუხებთ ქიმიური საწყობისა და იონური საწყობის იისფერი ფერები. წყლის შენახვა ხელმისაწვდომია ყველა კლასში და ჯგუფში. მიწისქვეშა წყლების პირველი საწყობი არის პირველი, რომელიც ინახება მათი ფორმირებისა და დაბინძურების გონებაში.
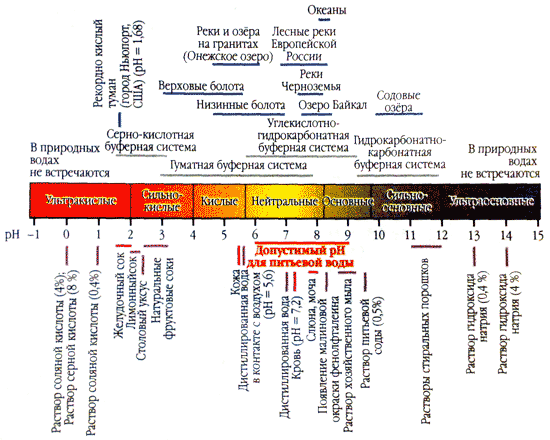
ბუნებრივი წყალი ინარჩუნებს pH მნიშვნელობას ნაკლებად სტაბილურს, რადგან ძლიერად ამცირებს მჟავას ან ფუძის მჟავიანობას. თუ ლიტრ გამოხდილ წყალს დაუმატებთ წვეთ კონცენტრირებულ მარილმჟავას, pH დაეცემა 7-დან 4-მდე. თუ წვეთ მარილმჟავას დაუმატებთ ლიტრ წყალს pH = 7, pH-ის მნიშვნელობა შეიძლება შეიცვალოს. მჟავები და ფუძეები, რომლებიც მოიხმარენ ბუნებრივ წყალს, ანეიტრალებს მასში გახსნილი ნახშირორჟანგი და ჰიდროკარბონატის იონები:
H + + HCO 3 - ↔ H 2 O + CO 2
OH - + CO 2 ↔ HCO 3 -
ჰიდროკარბონატის იონები ანეიტრალებს მჟავებს, რომლებიც იკარგება წყალში ატმოსფერული დეპონირების გზით ან წარმოიქმნება ორგანიზმების სიცოცხლისუნარიანობის შედეგად. წყლისა და მჟავე მჟავების წინააღმდეგობა პირდაპირ კავშირშია ჰიდროკარბონატის იონების კონცენტრაციასთან. მათ მიმართ ყველაზე მგრძნობიარე მდინარეებია კარელიის, ფინეთის, სკანდინავიის ტბები; მათ წყლებში პრაქტიკულად არ არის ასეთი იონები.
ბუნებრივი წყლების ორგანული მდინარე არის ორგანული რეზერვუარების მართლაც დაშლილი და კარგად ჩამოყალიბებული მდინარეების კომპლექსი. სიტუაციიდან გამომდინარე, ბუნებრივი წყლების ორგანული მდინარეები შეიძლება დაიყოს მდინარეებად, რომლებიც მიედინება სადრენაჟო ზონიდან და დაფუძნებულია წყლის ობიექტთან ახლოს. პირველ ჯგუფამდე მოდის ჰუმუსის ნარევების ძირითადი ნაწილი, რომელიც გამოირეცხება ნიადაგის წყლით, ტორფით, ტყის ჰუმუსით და სხვა სახის ბუნებრივი ხსნარებით, რომლებიც მოიცავს ჭარბ მცენარეებს და ორგანულ ნივთიერებებს, რომლებიც მოდის მრეწველობისა და მთავრობისგან. - ნარჩენი წყალი. ჰიდროქიმიისთვის ჰუმანურ მჟავებს შორის ყველაზე დიდი ინტერესია ჰუმუსური და ფულვის მჟავები. შემტევი მჟავები დამახასიათებელია ჰუმუსისთვის (ჰუმუს მჟავა), სუნი არ არის ცოცხალ მცენარეულ და ცხოველურ ქსოვილებში. მათ შორის ურთიერთობა სხვადასხვა ტორფსა და ნიადაგში განსხვავებულია. შავმიწა ნიადაგებში უფრო მნიშვნელოვანია ნეშომპალა მჟავები, ხოლო პოდზოლურ ნიადაგებში ფულვის მჟავები.
ორგანული ნივთიერებების კონცენტრაცია ბუნებრივ წყლებში, ფართო ინტერვალებით ცვალებადია, ყველაზე მაღალია ჭაობის წყლებში (რომელიც ჰუმუსის მაღალი კონცენტრაციით ზოგჯერ აღწევს 500 მგ/ლ ან მეტს) და მდინარეებში ჭაობის ტავერნებით, ხოლო ჭაობის წყალი არის დაბინძურებული ყავისფერი 300°-მდე და ფერთა მნიშვნელობის პლატინა-კობალტის მასშტაბის ზემოთ (ბუნებრივი წყლის დამატება ამატებს ჰუმინის მჟავებს). ორგანული მეტყველების ინოდის მაღალი კონცენტრაცია კონცენტრირებულია მიწისქვეშა წყლებინაფთა შემცველ საბადოებთან ასოცირდება კიდევ უფრო დიდი კონცენტრაცია შეიძლება წარმოიშვას სამრეწველო და საყოფაცხოვრებო ჩამდინარე წყლებით დაბინძურებულ ბუნებრივ წყლებში. დაუბინძურებელი ბუნებრივი წყლები იწვევს ორგანული ნივთიერებების მცირე ნაკადს. მაგალითად, ბ.ა. სკოპიცევის თქმით, ოკეანის წყალში ორგანული ნივთიერებების კონცენტრაცია ხდება 2,0-5,4 მგ/ლ-ზე ნაკლები (საშუალოდ 3,0 მგ/ლ, ხოლო მდინარის წყალში საშუალოდ 20 მგ/ლ).
ზოგიერთ ზედაპირულ წყლებში, განსაკუთრებით ჭაობის მდინარეებში, ჰუმუსის საბადოები წყლის ქიმიური შემადგენლობის ძირითად ნაწილს ქმნის. მას შემდეგ, რაც მდინარეები, შემდეგ კი ტბები და ზღვები კარგად აერირებს, წყლის ორგანული ნაწილები ექვემდებარება ცვლილებას, ხოლო ნიადაგებში, ჟანგვის პროცესი უმეტესწილად სრულდება მარტივი მინერალური ნივთიერებებიდან გადასვლით. მეორე, მდგრადი ნაწილი იკარგება და გროვდება წყლის ობიექტებში.
ცივ კლიმატურ ზონებში (ტუნდრა) ძალიან ცოტაა ორგანული ჭარბი და იქ წყლის რეზერვუარები შეიძლება არ შეიცავდეს ჰუმინის მჟავებს. ხოლო ტყეების ზონაში, განსაკუთრებით წიწვოვანებში, სადაც ორგანული ნარჩენები უხვადაა და სუნი ზედაპირზე არ იშლება, ჰუმინის მჟავების ნაცვლად ლიტრზე რამდენიმე ათეული მილიგრამია. ჰუმინის მჟავები არა მხოლოდ ამჟავებს წყალს წყალსაცავში, არამედ აკავშირებს კომპლექსის თითქმის ყველა მნიშვნელოვან ლითონს.
როცა ონკანიდან ცივ წყალს ბოთლში ჩაასხამთ და თბილ ადგილას მოათავსებთ, კედლებზე გაზის ბუშტები გამოჩნდება. გაზი განადგურდა ცივი წყალიდა შესამჩნევი იყო გაცხელებისას (გაზების კონცენტრაცია იცვლება გაცხელებისას). ეს არის მჟავე აირი, აზოტი და ნახშირორჟანგი. წყალში გაზის ინტენსივობა მცირდება ტემპერატურის მატებასთან ერთად, რაც დაკავშირებულია გაზის მოლეკულების კინეტიკური ენერგიის ზრდასთან, რაც ამცირებს წყლის მოლეკულების გრავიტაციულ ძალებს. ყველა ბუნებრივი წყალი წარმოადგენს გაზის წყაროს. ჟანგბადი O 2 და ნახშირორჟანგი CO 2 ყველაზე მეტია ზედაპირულ წყლებში, ხოლო ჟანგბადი H 2 S და მეთანი CH 4 ყველაზე მეტად მიწისქვეშა წყლებშია. მნიშვნელოვანი რაოდენობით, CO 2 ასევე შეიძლება იყოს წყალში ღრმა ჰორიზონტიდან. გარდა ამისა, ყველა ბუნებრივი წყალი მუდმივად შეიცავს აზოტს N2.
კისენი (O 2)ნაპოვნია ბუნებრივ წყალში გატეხილი მოლეკულების გამოჩენაში. კისენი, როგორც ძლიერი ჟანგვის აგენტი, განსაკუთრებულ როლს ასრულებს ბუნებრივი წყლების ქიმიური შენახვის ფორმირებაში. კისენი წყლიდან მოდის ფოტოსინთეზის პროცესების შედეგად, რომლებიც ხდება ბუნებაში და ატმოსფეროდან. კისენი გამოიყენება ორგანული ნივთიერებების დაჟანგვისთვის, ასევე ორგანიზმების გადაგვარების პროცესში. გახსნილი მაწონის კონცენტრაცია ბუნებრივ წყლებში მერყეობს 0-დან 14 მგ/ლ-მდე, ინტენსიური ფოტოსინთეზით, ეს უკანასკნელი, შესაძლებელია და უფრო მაღალი კონცენტრაციით. დაბალი ფაქტორების გამო ზედაპირულ წყლებში მჟავის ხანგრძლივი კონცენტრაციის გამო, მისი კონცენტრაცია მნიშვნელოვნად იცვლება წარმოების ხანგრძლივობის, სეზონისა და ბედისწერის მიხედვით. მკვდარი მჟავიანობის ნარჩენები ნაკლებად სავარაუდოა, რომ დარჩება მზის რადიაციის ცვლილებების გამო და ფოტოსინთეზი მთლიანად მასზეა დამოკიდებული; დღის მატებასთან ერთად მჟავიანობა გროვდება და ბნელი საათი საშუალებას აძლევს მას მოხმარდეს. მაწონი აუცილებელია წყლებში მცხოვრები ორგანიზმების უმეტესობის განადგურებისთვის. როგორც ძლიერი ჟანგვის მჟავა, ის მნიშვნელოვან სანიტარულ და ჰიგიენურ როლს ასრულებს, ხელს უწყობს ორგანული ჭარბი მინერალიზაციის სწრაფ მინერალიზაციას.
ნახშირორჟანგი (CO2)უნდა იყოს პასუხისმგებელი წყალზე, რათა დაინახოს მოლეკულების დაშლა CO2 გაზად. თუმცა, მისი ნაწილი (დაახლოებით 1%) ურთიერთქმედებს წყალთან, ხსნის ნახშირმჟავას:
CO 2 + H 2 O ↔ H 2 CO 3
დარწმუნდით, რომ არ დაამატოთ CO 2 და H 2 CO 3 და ნახშირორჟანგის ზედმეტად (CO 2 + H 2 CO 3). ბუნებრივ წყლებში ნახშირორჟანგი იმყოფება ორგანული ნივთიერებების დაჟანგვის პროცესამდე, რაც გამოწვეულია CO 2-ის არსებობით როგორც წყალში, ასევე ნიადაგებსა და ზედაპირებზე, რომლებზეც წყალი მიედინება. მათ წინ ისმის წყლის ორგანიზმების სუნთქვა და განსხვავებული შეხედულებებიორგანული ნარჩენების ბიოქიმიური დაშლა და დაჟანგვა. ზოგიერთ მიწისქვეშა წყლებში არის ნახშირორჟანგისა და ვულკანური გაზების მნიშვნელოვანი წყარო, რომელიც ჩანს მიწის ზემოთ, რომლის გაჩენა დაკავშირებულია მანტიის გაჟონვასთან და დანალექი ფორების მეტამორფოზის რთულ პროცესებთან, რომლებიც ხდება იქ. თიხა შემოდინების ქვეშ მაღალი ტემპერატურა. ამიტომ, ნახშირორჟანგის მაღალ დონეს ხშირად ერიდებიან მიწისქვეშა წყლებში და თიხიან წყალსაცავებში. წყლის მიერ ატმოსფეროდან ნახშირორჟანგის გამოყოფა უფრო მნიშვნელოვანია ზღვისა და ოკეანის წყლებისთვის და ნაკლებად მნიშვნელოვანია ხმელეთის წყლებისთვის. ნახშირორჟანგის ჩანაცვლება ნახშირორჟანგით ხდება ფოტოსინთეზის დროს. ინტენსიური ფოტოსინთეზის დროსაც კი, თუ შემცირდა გაზის მსგავსი CO 2, დარჩენილი იონები შეიძლება ნახოთ HCO 3 - იონებიდან:
HCO 3 - ↔ CO 3 2- + CO 2
ნახშირორჟანგი ასევე გამოიყენება კარბონატების დასაშლელად:
CaCO 3 + CO 2 + H 2 O ↔ Ca(HCO 3) 2
ასევე გამოიყენება ალუმინოსილიკატების ქიმიური ვიტრიფიკაცია. წყალში CO 2-ის ცვლილება, განსაკუთრებით ხმელეთზე ზედაპირულ წყლებში, ასევე შეინიშნება ატმოსფეროში გაშვებისას. წვის CO 2 ატმოსფეროს დიდი მნიშვნელობა აქვს CO 2-სთვის, რომელიც ბინადრობს ზედაპირულ წყლებში და არეგულირებს მას იქ. CO 2 ატმოსფეროსა და CO 2 ზედაპირულ წყლებს შორის მიმდინარეობს უწყვეტი გაცვლა, რაც მიმართულია მათ შორის თანაბარი ბალანსის დამყარებას ჰენრი-დალტონის კანონის საფუძველზე. ნახშირორჟანგის ნაწილობრივი წნევა ატმოსფეროში ძალიან მცირეა (33 Pa), მაშინ, მიუხედავად მისი დიდი სიძლიერისა (1013 hPa წნევის დროს და 12 °C ტემპერატურაზე 2166 მგ/ლ-მდე), ბალანსი. წყალსა და ატმოსფეროს შორის მიიღწევა წყალში CO 2-ის ძალიან მცირე რაოდენობით. CO 2-ის ნაწილობრივი წნევის დროს ატმოსფეროში 33 Pa, მისი კონცენტრაცია წყალში იქნება 2166.0.00033 = 0.715 მგ/ლ (12 °C-ზე). მიწის ზედაპირული წყლების გამო, რომლებშიც მიმდინარეობს ორგანული ნივთიერებებისა და ნიადაგების დაშლის სხვადასხვა პროცესები, უფრო დიდი რაოდენობით CO 2 ხორციელდება და ამიტომ გამოიყოფა ატმოსფეროში. თუ ფოტოსინთეზი არ არის ძალიან ძლიერი, თუ CO 2 იმყოფება, CO 2 შეიძლება ამოღებულ იქნეს ატმოსფეროდან. ბუნებრივ წყლებში ნახშირორჟანგის ნაცვლად ის უკიდურესად ცვალებადია - რამდენიმე მეათედამდე 3000-4000 მგ/ლ-მდე. CO 2-ის ყველაზე დაბალი კონცენტრაცია შეინიშნება ზედაპირულ წყლებში, განსაკუთრებით მინერალიზებულ წყლებში (ზღვა, მარილიანი ტბები), ყველაზე მაღალი მიწისქვეშა და დაბინძურებულ ჩამდინარე წყლებში. მდინარეებსა და ტბებში CO 2 კონცენტრაცია იშვიათად აღემატება 20-30 მგ/ლ.
როზჩინის მოლეკულური აზოტი (N 2)- ყველაზე სტაბილური გაზი ბუნებრივ წყლებში. ქიმიურად ყველაზე სტაბილური და ბიოლოგიურად მნიშვნელოვანი აზოტი, რომელიც შედის ოკეანეში ან მიწისქვეშა წყლებში თიხის ბურთებში, სწრაფად იცვლება მხოლოდ ფიზიკური ძალების შემოდინებით (ტემპერატურა და წნევა). ზედაპირული წყლების შემთხვევაში აზოტი მნიშვნელოვან როლს ასრულებს წყალმომარაგებაში. ბუნებაში ფართოდ არის გავრცელებული ბიოგენური აზოტის მატება, რაც გამოწვეულია დენიტრიფიკაციის შედეგად.
გაზი მეთანი (CH4)აღწევს უდიდეს გაზებსა და მიწისქვეშა წყლებს. მიწისქვეშა წყლების გაზის ფაზაში ხშირად ჭარბობს აზოტი, ნახშირორჟანგი ან მეთანი. მეთანის შექმნის ძირითადი წყაროა ქანებში დისპერსიული ორგანული ნაერთები. მეთანი, რომელიც მნიშვნელოვანია ნახშირწყლებში, ხშირად გვხვდება მნიშვნელოვანი კონცენტრაციით დახურული სტრუქტურების ღრმა მიწისქვეშა წყლებში, რომლებიც დაკავშირებულია ნაფტას შემცველ საბადოებთან. დაბალ კონცენტრაციებში მეთანი გროვდება ბუნებრივ ტბებში, სადაც მისი დანახვა შესაძლებელია ჯორიდან მაღალი ხეების გაშენებისას, ასევე ოკეანის ფსკერის საბადოებში მაღალი ბიოლოგიური პროდუქტიულობის ადგილებში.
გაზი სირკვოდენი (H 2 S)ეს არის ცილოვანი ნივთიერების დაშლის ერთ-ერთი პროდუქტი, რომელიც ინახება თქვენს საწყობში და, შესაბამისად, მისი დაგროვება ხშირად ინახება წყალთან ერთად ქვედა ბურთებში სხვადასხვა ორგანული ჭარბი ლპობის გამო. ღრმა ტბებისა და ზღვების ქვედა ნაწილებში, სადაც ხდება წყლის ყოველდღიური გაცვლა, ხშირად ვითარდება ღრმა წყლის ზონა. ატმოსფეროში წყლის ნაწილობრივი წნევით ნულის ქვემოთ, ზედაპირულ წყლებში წყლის არსებობა შეუძლებელია. გარდა ამისა, ღვინო იჟანგება მჟავიანობით, რომელიც იხსნება წყლით. მდინარეებში ღრმა წყალი შემოიფარგლება ძირითადად ქვედა აუზებით, განსაკუთრებით ზამთრის პერიოდში, როდესაც წყლის სხეულის აერაცია რთულია. ბუნებრივ, დაუბინძურებელ ზედაპირულ წყლებში წყლის წყლის არსებობა იშვიათი მოვლენაა. უფრო ხშირად, ვიდრე არა, წყალი იმყოფება მიწისქვეშა წყლებში, რომლებიც იზოლირებულნი არიან ზედაპირიდან და ძლიერ დაბინძურებულ ზედაპირულ წყლებში, რომლებშიც ღვინოები ძლიერი დაბინძურების და ანაერობული დრენაჟის მაჩვენებელია.
წყალში არსებული ელემენტების გარდა, რამდენიმე ელემენტი: აზოტი, ფოსფორი, სილიციუმი, ალუმინი, ნერწყვი, ფტორი იმყოფება კონცენტრაციებში 0,1-დან 10 მგ/ლ-მდე. სუნი ეწოდება მეზოელემენტებს (ბერძნულიდან "Mesos" - "შუა", "შუალედური").
აზოტი ნიტრატების სახით NO 3 - იკარგება წყალში და სუფრის წყალში, ხოლო ამინომჟავების, მარილების (NH 2) 2 CO და ამონიუმის მარილების NH 4 + სახით - ორგანული ჭარბი მოხმარებისას.
ფოსფორი წყალში იმყოფება ჰიდროფოსფატების HPO 3 2- და დიჰიდროგენოფოსფატების H 2 PO 3 - ორგანული ჭარბი დაშლის შედეგად წარმოქმნილი სახით.
სილიციუმი ბუნებრივი წყლების ქიმიური შენახვის აუცილებელი კომპონენტია. ეს განპირობებულია მთიან ქანებში სილიციუმის არსებობით ყველგან სხვა კომპონენტების არსებობით, ხოლო დარჩენილი კომპონენტების მცირე მრავალფეროვნება ხსნის სილიციუმის მინიმალურ შემცველობას სასმელ წყალში. სილიციუმის კონცენტრაცია ბუნებრივ წყლებში არის რამდენიმე მილიგრამი 1 ლიტრზე. მიწისქვეშა წყლებში ის ადის და ხშირად ეცემა ათეულ მილიგრამამდე 1 ლიტრზე, ხოლო ცხელ თერმულ წყლებში - ასეულამდე. ტემპერატურის გარდა, სილიციუმის მგრძნობელობაზე ძლიერ გავლენას ახდენს pH ცვლილებები. ზედაპირულ წყლებში არის მცირე რაოდენობით სილიციუმი, რომელიც მცირდება სილიციუმის დიოქსიდამდე (125 მგ/ლ 26 °C-ზე, 170 მგ/ლ 38 °C-ზე), რაც მიუთითებს წყალში პროცესების არსებობაზე, რომლებიც ცვლის მის კონცენტრაციას. მათ წინაშე აუცილებელია სილიკონით მდიდარი წყლის ორგანიზმების შემოღება, რომელთაგან ბევრი, მაგალითად, დიატომის წყალმცენარეები, შექმნის მათ სილიკონის ჩონჩხს. გარდა ამისა, სილიციუმის მჟავა, როგორც სუსტი მჟავა, განსხვავდება ნახშირბადის მჟავისგან:
Na 4 SiO 4 + 4CO 2 + 4H 2 O = H 4 SiO 4 + 4NaHCO 3
ამცირებს სილიციუმის არასტაბილურობას სილიციუმის მჟავას გელად გადაქცევის ტენდენციის გამო. ძალიან მცირე მინერალიზებულ წყლებში სილიციუმი ხდება წყარო და ზოგჯერ წყლის ქიმიური შემადგენლობის მნიშვნელოვანი ნაწილი, საერთოდ არ აქვს მნიშვნელობა. წყალში სილიციუმის არსებობა ტექნოლოგიის სერიოზული დეფექტია, რადგან მდუღარე წყალი მთლიანად მშრალია, სილიციუმი ქმნის ძალიან ხისტ სილიკატურ ქილას ქვაბებში.
ალუმინი წყალთან ახლოს არის თიხაზე მჟავების (კაოლინის) არსებობის გამო:
Al 2 (OH) 4 + 6H + = 2SiO 2 + 5H 2 O + 2Al 3+
ძირითადი საბადო თიხაა. ორგანული ნარჩენები (შემდგომში „C“), მათთან შეხებისას ამცირებენ შემცველობას ორვალენტიანამდე, რომელიც მთლიანად შეიწოვება ჰიდროკარბონატის ან ჰუმინის მჟავების მარილების სახით:
2Fe 2 O 3 + "C" + 4H 2 O + 7CO 2 = 4Fe(HCO 3) 2
როდესაც დაშლილი Fe 2+ იონების წყალი შედის წყალთან კონტაქტში, ის სწრაფად იჟანგება და წარმოქმნის Fe(OH) 3 ჰიდროქსიდის ყავისფერ ნალექს. წელს იგი გადაკეთებულია ჭაობის მადნად - ყავისფერ სარეველად (ლიმონიტი) FeO(OH). კარელიის ჭაობის მადანი მოიპოვებოდა მე-18-19 საუკუნეებში გარსის მოსაპოვებლად.
წყლის ზედაპირზე ცისფერი ლაქა არის Fe(OH) 3, რომელიც იხსნება, როდესაც მიწისქვეშა წყალი, რომელიც შეიცავს Fe 2+ იონებს, შედის ზედაპირთან კონტაქტში. ისინი ხშირად იკარგებიან პოლიეთილენის დნობაში, მაგრამ მათი დაჭრა ძალიან მარტივია: ჰიდროქსიდის დნობა მოშუშებს მოწყვეტილ კიდეებს. მას შემდეგ, რაც სითხე წყლის ზედაპირზე მოხვდება, გაწურეთ დნობის ჰიდროქსიდი ზეთის ქვაბში, ისე, რომ არ გადმოვიდეს.
ამ ჯგუფში შედის ელემენტები, რომლებიც გვხვდება ბუნებრივ წყლებში ძალიან მცირე კონცენტრაციით, ამიტომ მათ მიკროელემენტებს უწოდებენ. მათი კონცენტრაცია იცვლება მიკროგრამებში 1 ლიტრზე (მკგ/ლ) და ხშირად უფრო დიდი მნიშვნელობები აქვს. მიკროელემენტები არის ელემენტების უდიდესი ჯგუფი ბუნებრივი წყლების ქიმიურ შემადგენლობაში; ისინი მოიცავს პერიოდული სისტემის ყველა ელემენტს, რომლებიც არ შედის განხილული კომპონენტების წინა ჯგუფებში. ისინი გონებრივად შეიძლება დაიყოს ხუთ ქვეჯგუფად: 1) ტიპიური კათიონები (Li +, Rb +, Cs +, Be 2+, Sr 2+, Ba 2+ და ასე შემდეგ); 2) მნიშვნელოვანი ლითონების იონები (Cu 2+, Ag +, Au +, Pb 2+, Fe 2+, Ni 2+, Co 2+ და ასე შემდეგ); 3) ამფოტერული კომპლექსები (Cr, Mo, V, Mn); 4) ტიპიური ანიონები (Br -, I -, F -); 5) რადიოაქტიური ელემენტები. მიკროელემენტები აუცილებელია მცენარეების, ცხოველებისა და ადამიანების ნორმალური ცხოვრებისათვის. თუმცა, გაზრდილი კონცენტრაციით, ბევრი მიკროელემენტი საზიანო და მავნეა ცოცხალი ორგანიზმებისთვის. ამიტომ სუნი ხშირად დნება ტალახიან ბგერებში და მათი კონცენტრაცია კონტროლდება. მიკროელემენტების წარმატებული კულტივირება რთულია ბუნებრივ წყლებში მათი მცირე ყოფნისა და წყლებში მათი ყოფნის ფორმის დიდი გაურკვევლობის გამო. ძნელია მათი მიგრაციისა და რეჟიმის ნიმუშების ახსნა და ქმნის სირთულეებს ქიმიურ ანალიზში. მაგალითად, ბევრი მნიშვნელოვანი ლითონებიისინი მაღალი კონცენტრაციით მიგრირებენ სასიცოცხლო მდგომარეობაში და არა უწესრიგო მდგომარეობაში. დაშლილი ორგანული კომპლექსები ქმნის მეტალების უმეტესობას, პირველ რიგში სამვალენტიან ლითონებს ჰუმუსური და ფულვის მჟავებით. კომპლექსური ლითონების კონცენტრაცია გამოითვლება ორგანული მჟავების კონცენტრაციამდე. ქანების გარეგნობა მდიდარია ლითონის ჰიდროქსიდებით. შესაძლებელია, რომ მოხდეს ორგანული ნივთიერებების ადსორბცია კოლოიდების ზედაპირზე, რაც მათ უფრო მეტ სტაბილურობას აძლევს დაშლისას.
ქიმიური საწყობიბუნებრივი წყალი ნიშნავს წინა ისტორიას, მაშინ. წყლის მიერ მისი მიმოქცევის პროცესში წარმოქმნილი ბილიკები. ამგვარ წყალში მრავალი განსხვავებული გამოსვლები დეპონირებულია, ერთის მხრივ, ამ გამოსვლების საწყობიდან, რომლითაც იგი მიედინებოდა, მეორეს მხრივ - გონებიდან, რომლითაც ისინი ურთიერთობდნენ ერთმანეთთან. ქიმიურ რეზერვუარს შეუძლია წყლის დამატება შემდეგი ფაქტორებით: მთიანი ქანები, ნიადაგები, ცოცხალი ორგანიზმები, ადამიანის აქტივობა, კლიმატი, რელიეფი, წყლის რეჟიმი, მცენარეულობა, ჰიდროგეოლოგიური და ჰიდროდინამიკური პირობები და ა.შ. მოდით უფრო დეტალურად განვიხილოთ ფაქტორები, რომლებიც მიედინება წყლის საცავში.
ნიადაგის დაშლა და ატმოსფერული ჩამონადენი, რომელიც იფილტრება ნიადაგში, იწვევს ქანების და მინერალების დაშლას. ეს არის ერთ-ერთი ყველაზე მნიშვნელოვანი გავლენა ნიადაგზე, რომელიც მიედინება ბუნებრივი წყლების ჩამოსხმის საწყობში, რის შედეგადაც იზრდება ნახშირორჟანგის კონცენტრაცია ნიადაგში, რაც ჩანს ნიადაგში ცოცხალი ორგანიზმების და ფესვთა სისტემების გამოშრობისა და ბიოქიმიური რღვევის დროს. ორგანული ჭარბი რაოდენობით. შედეგად, CO 2-ის კონცენტრაცია ნიადაგის ჰაერში იზრდება 0,033%-დან ატმოსფერულ ჰაერში, 1%-მდე ან მეტზე ნიადაგის ჰაერში (მნიშვნელოვან თიხიან ნიადაგებში CO 2-ის კონცენტრაცია ნიადაგის ჰაერში ქარი აღწევს 5-ს. -10%, რითაც აძლევს ძლიერ აგრესიულ მოქმედებას ასაკის მიხედვით ჯიშებს). კიდევ ერთი ფაქტორი, რომელიც აძლიერებს ნიადაგში გაფილტრული წყლის აგრესიულ ეფექტს, არის ორგანული ნივთიერებები - ნიადაგის ჰუმუსი, რომელიც ყალიბდება ნიადაგში ჭარბი მცენარეულობის ტრანსფორმაციის დროს. აქტიური რეაგენტების ჭურჭელში ჰუმუსის შენახვისას ჯერ უნდა დავასახელოთ ჰუმუსური და ფულვის მჟავები და მარტივი ნივთიერებები, როგორიცაა ორგანული მჟავები (ლიმონის, მჟავე, ოქსიტოინის, ვაშლის და სხვ.). ორგანული მჟავებითა და CO 2-ით მდიდარი ნიადაგის მოპოვება ხშირად აჩქარებულია ნიადაგში განლაგებული ალუმინის სილიკატების ქიმიური ვიტრიფიკაციით. ანალოგიურად, წყალი, რომელიც იფილტრება ნიადაგში, აჩქარებს ალუმინისილიკატების და კარბონატული ქანების ქიმიურ ვიბრაციას, რომლებიც ნიადაგის საფუძველშია. ვაპნიაკი ადვილად ხსნის დაბალი ხარისხის (1,6 გ/ლ-მდე) კალციუმის ჰიდროკარბონატს:
CaCO 3 + H 2 O + CO 2 ↔ Ca(HCO 3) 2
რუსეთის მთელ ევროპულ ნაწილში (კარელიის ყირიმი და მურმანსკის რეგიონი) საბადოები, ისევე როგორც დოლომიტი MgCO 3 .CaCO 3, მდებარეობს ზედაპირთან ახლოს. აქედან გამომდინარე, აქ წყალი მნიშვნელოვანია, რომ შეიცავდეს კალციუმს და მაგნიუმის ჰიდროკარბონატს. მდინარეებში, როგორიცაა ვოლგა, დონე, პივნიჩნა დვინა და მათი ძირითადი ნაკადები, კალციუმი და მაგნიუმის ჰიდროკარბონატი ხდება ყველა გახსნილი მარილის 3/4-დან 9/10-მდე.
მარილები მოიხმარება წყლის ობიექტებიდან და ადამიანის საქმიანობის შედეგად. ასე რომ, გზებს ასხურებენ ნატრიუმის და კალციუმის ქლორიდებით ყინულის დნობის მიზნით. გაზაფხულზე, ქლორიდები ერთად მიედინება მდ. რუსეთის ევროპული ნაწილის მდინარეებში ქლორიდების რაოდენობა იქ ადამიანებმა შემოიტანეს. მდინარეებთან, რომლებზეც დიდი ადგილები დგას, ეს ნაწილი უფრო მდიდარია.
უბნის რელიეფი ირიბად ავსებს წყლის რეზერვუარს, შთანთქავს ნიადაგიდან მარილების მოცილებას. მდინარის ეროზიული ჭრილის სიღრმე აადვილებს მდინარემდე მისვლას უფრო მინერალიზებული მიწისქვეშა წყლებით ქვედა ჰორიზონტებიდან. ვის ეტევა სხვა სახის დეპრესიები (მდინარის ხეობები, ხეობები, ხევები), რომლებიც აუმჯობესებენ წყალგამყოფის დრენაჟს.
კლიმატი ქმნის მხურვალე ფონს, რაც საშუალებას იძლევა უფრო დიდი რაოდენობის პროცესები მოხდეს ბუნებრივი წყლების ქიმიური რეზერვუარის ფორმირებაში. კლიმატი უპირველეს ყოვლისა დამოკიდებულია სითბოს და წყლის ბალანსზე, რომელიც განსაზღვრავს ნიადაგის საბადოებს და წყლის ნაკადის მოცულობას და, შესაბამისად, ბუნებრივი დარღვევების განზავებას ან კონცენტრაციას და მდინარეების განადგურების ან მათი ალყის ქვეშ მოქცევის შესაძლებლობას.
ძალიან მნიშვნელოვანია წყლის ქიმიური საწყობის დიდი ნაკადის მიღება და წყლის სხეულის სიცოცხლისა და მისი ურთიერთობის დროთა განმავლობაში შეცვლა. თოვლის დნობის პერიოდში მდინარეებში, ტბებსა და წყალსაცავებში წყალს უფრო დაბალი მინერალიზაცია აქვს, იმ პერიოდში, როდესაც სიცოცხლის უმეტესი ნაწილი მიწისქვეშა და მიწისქვეშა წყლებიდან მოდის. ამიტომ ავეჯს იყენებენ წყლის ზედაპირის რეგულირებისა და მათგან წყლის ამოღებისას. როგორც წესი, სანიაღვრე აუზები ივსება გაზაფხულის სეზონზე, თუ მოქცევის წყალს ნაკლები მინერალიზაცია აქვს.
წყლის ქიმიური შენახვა შეიძლება განსხვავებული იყოს და ფრაგმენტები შეიძლება იყოს არაორგანული და ორგანული ნივთიერებების ნაწილაკების ადგილზე. დედამიწის სხვადასხვა ნაწილში მიედინება წყალი არღვევს მათში არსებულ მარილებს (კალციუმს, მაგნიუმს და ა.შ.).
დედამიწის ზედაპირზე ბრუნვისას წყალი გროვდება გაზებით, ხსნის მათ. ბუნებრივი წყლები ქიმიური საწყობიდან გამოყოფილია ერთი ტიპით, ისე რომ ისინი წარმოიქმნება გაზებით, ძირითადი იონებით, ბიოგენური და ორგანული ნივთიერებებით და მიკროელემენტებით.
წყლისა და ქიმიკატების დიდი ნაკადი გამოიყენება ნიადაგსა და საწოლზე. წყალი ნიადაგიდან აშორებს მინერალურ და ორგანულ ნივთიერებებს, რაც განსაკუთრებით საგულდაგულოდ არის დაცული ექსპლუატაციის პირველ ეტაპებზე.
ბუნებრივი და ხელოვნური რეზერვუარების გაზის რეჟიმი იქმნება ატმოსფეროდან და ქიმიური პროცესების შედეგად დაკარგული აირების კომბინაციით. დაშლილი გაზების დიდი რაოდენობა რჩება ტემპერატურის, წნევის და წყალში მარილების არსებობის გამო.
ეს აირები და უპირველეს ყოვლისა მჟავიანობა და ნახშირორჟანგი უბრალოდ აუცილებელია წყლის ორგანიზმების სიცოცხლისთვის. რაც უფრო მეტია წყალთან ახლოს, მით უკეთესია წყლის აუზში მყოფი ადამიანებისთვის. თუმცა წყლის, მეთანისა და აზოტის მაღალი შემცველობა ამცირებს ცოცხალი არსებების სიცოცხლისუნარიანობას.
ერთ-ერთი ყველაზე მნიშვნელოვანი აირი, რომელიც მუდმივად იმყოფება ზედაპირულ წყლებში, არის მაწონი. წყლის მნიშვნელოვანი რაოდენობა გვხვდება ქიმიურ-ბიოლოგიურ წყლებში.
თავაძრელებს აავსებენ მჟავე წყლით
- ატმოსფერო - ამომავალი ქარის ქვეშ, ერწყმის წყლის ზედაპირულ ბურთებს;
- მიკროსკოპული წყალმცენარეების ფოტოსინთეზი.
მაღალ ტემპერატურაზე წყლის მჟავიანობა იცვლება, დაბალ ტემპერატურაზე კი მატულობს.
ბუნებრივ წყლებში წყლის მჟავიანობა 100%-ზე ნაკლებია, რადგან ამ გაზის მოცულობა გადადის ორგანული ნივთიერებების დაჟანგვაში. როდესაც წყალმცენარეების მასიური განვითარებაა (ადრეულ დღეებში) დიდ წყალში, მჟავიანობამ შეიძლება მიაღწიოს 150-200%-ს.
ნახშირორჟანგი (CO 2) დიდი რაოდენობითაა ყველა ბუნებრივ წყალში. ამ შემთხვევაში ნახშირორჟანგის უმეტესობა იმყოფება გახსნილ მდგომარეობაში და ნახშირორჟანგის მცირე რაოდენობას (1%-მდე) შეუძლია წყალთან ურთიერთქმედება და ნახშირბადის მჟავის შექმნა.
ნახშირმჟავას კონცენტრაციის ზრდა ნარევში ოპტიმალური დონისთვის ეფუძნება ორგანული ნივთიერებების კონცენტრაციას. განსაკუთრებით მნიშვნელოვანია მჟავიანობის და ნახშირმჟავას წარმოების რეგულირება.
წყლის ქიმიური შემადგენლობის და მისი ცვლილების ხასიათის დასადგენად უნდა ჩატარდეს ლაბორატორიული გამოკვლევები. წყლის მჟავიანობის შესახებ ძირითადი ინფორმაციის მიღება შესაძლებელია სპეციალური მოწყობილობის გამოყენებით, რომელიც გამოიყენება ტესტირებისთვის. არის გამჭვირვალე ბლოკი ორი თხრილით და ფერის მასშტაბით.
ამ და სხვა ქიმიკატების თანდასწრებით, წყალი, რომელიც ტესტირება ხდება, ავითარებს მკაფიო ფერს, რომელიც ემთხვევა სასწორის ფერთა შკალას. კანის ფერის მასშტაბი განისაზღვრება წყლის მჟავიანობის დონით.
წყლის მჟავიანობა (pH) ახასიათებს მედიის აქტიურ რეაქციას. რაც უფრო ახლოს არის pH მნიშვნელობა ნულთან, რაც უფრო მაღალია წყლის იონების კონცენტრაცია ხსნარში, მით უფრო მჟავეა შუა.
ადამიანებისთვის წყლის მჟავიანობის ოპტიმალური მაჩვენებელი 7,2-7,4-ის ვიწრო დიაპაზონშია, მაქსიმუმ 7,6. ასეთი თანაბარი pH-ით წყალი არ მიედინება ადამიანის კანზე და ხელს უშლის მიკროორგანიზმების გამრავლებას.
თუ pH მნიშვნელობა 7,8-ზე მაღალია, ასეთი წყალი აღიზიანებს კანს (განსაკუთრებით მგრძნობიარე) და მიკროორგანიზმები ადვილად მრავლდებიან წყალში. გარდა ამისა, მაღალი რევანდი pH ხელს უწყობს წყლის კოროზიულ აქტივობას, რაც მნიშვნელოვნად მოქმედებს ფლობისა და კომუნიკაციის ეფექტურობაზე.
წყლის pH-ის ყველაზე მაღალი დონე (8-8,8) შეინიშნება ვეგეტაციის მეორე ნახევარში, როდესაც წყალმცენარეების ბიომასა აღწევს უდიდეს განვითარებას და ფოტოსინთეზის პროცესები მიმდინარეობს მაქსიმალური ინტენსივობით.
წყლის მსგავსი ქიმიური რეაქციების შედეგად. pH დონე თანდათან იცვლება, როგორც წყალთან, ასევე მიღებულ წყალთან ერთად.
წყლის სიმკაცრე დიდად მოქმედებს pH დონეზე. დიახ, y რბილი წყალირევანდის pH 7.0-ზე ნაკლებია, მწარეს კი შეიძლება 9.0-ს მიაღწიოს.
წყლის სიხისტე განისაზღვრება Ca CO2-ის ნაცვლად (). როდესაც ხდება ტემპერატურის ცვლილებები, ნალექი ეცემა აუზის კედლებს, ფილტრებს, სითბოს გადამცვლელებს და სხვა მოწყობილობებს.
სტანდარტების მიხედვით წყლის სიხისტე არ უნდა აღემატებოდეს 30°dH-ს, სადაც 1°dH = 10 მგ CaO/l. წყლის სიმტკიცე შეიძლება შეიცვალოს დიდი ხნის განმავლობაში დგომისას. ზამთარში, წვიმების დროს ის უფრო მცირდება.
წყლის დაჟანგვა განისაზღვრება სხვადასხვა ორგანული და მინერალური ნივთიერებების გამოყენებით.
ჟანგვის რაოდენობა გვიჩვენებს, თუ რამდენ ჟანგვას იკარგება ორგანული ნივთიერებების განადგურებისას (მგ/ლ). მიმდინარე ვეგეტაციის პერიოდში წყლის დაჟანგვა იცვლება 10-დან 30 მგ-მდე 1 ლიტრზე ან მეტზე.
ქიმიური წყლის საწყობი. ბუნებაში ჩვეულებრივია წყალი ყოველთვის შეიცავს მეტ-ნაკლებად მის მინერალურ მარილებს. ნაბიჯი მინერალების საწყობიწყალი განისაზღვრება ნიადაგის ან ნიადაგების ბუნებით, რომლებიც დევს წყალსატევებზე ან ზედაპირული წყლის რეზერვუარებში.
მინერალური მარილების რაოდენობა, ისევე როგორც წყალი, გამოხატულია მგ/ლ-ში.
ორგანული გამოსვლები. მათგან ყველაზე მნიშვნელოვანია არსების მოგზაურობის სიტყვები, სუნის ფრაგმენტები შეიძლება შეიცავდეს სხვადასხვა პათოგენურ მიკრობებს. წყალში ამ ნივთიერებების არსებობის ან არსებობის არაპირდაპირი ჰიგიენური მაჩვენებელია წყლის დაჟანგვა.
წყლის დაჟანგვა. მჟავიანობის რაოდენობა (მგ), რომელიც იხარჯება ორგანული ნივთიერებების გარე დაჟანგვაზე, რომელიც შეიცავს 1 ლიტრ წყალში (მითითებულია მგ/ლ). რაც უფრო მცირეა მჟავიანობა წყალში, მით უფრო მცირეა მჟავიანობის რაოდენობა ორგანული ნაერთებით 1 ლიტრ წყალში დაჟანგვის ზედაპირზე. მაგალითად, სუფთა მიწისქვეშა წყლების დაჟანგვა არის არაუმეტეს 2-4 მგ/ლ, მდინარის წყალი არაუმეტეს 7 მგ/ლ.
წყალში ორგანული მჟავების შესაძლო არსებობის ერთ-ერთი მაჩვენებელია მასში გახსნილი მჟავიანობის რაოდენობა (მგ). სუფთა წყლებში გამოიყოფა 3-6 მგ/ლ მჟავე წყალი, ხოლო დაბინძურებულ წყლებში სრულ არარსებობამდე გაცილებით ნაკლები.
ამიაკის, აზოტის მარილების და აზოტის მჟავების არსებობა შეიძლება შეინიშნოს ამიაკის, აზოტის მარილების და აზოტის მჟავების არსებობისას. ამიაკი არის პროდუქტი cob ეტაპებიორგანული ნარჩენების გაფუჭება სამზარეულოდან, აზოტისა და აზოტის მჟავების მარილები ორგანული ნარჩენების მინერალიზაციის საბოლოო პროდუქტია. აშკარაა, რომ წყალი დიდი ხნის განმავლობაში იყო შეფერხებული.
წყალში ჰიდროქლორინის და მჟავე მჟავების მარილების არსებობა მიუთითებს წყლის შესაძლო დაბინძურების შესახებ ცხოველებისა და ადამიანების ექსკრემენტებით (ფეკალური დაბინძურება). განვიხილოთ 1 ლიტრი სუფთა ბუნებრივი წყალი, რომელიც შეიცავს 20-30 მგ-ზე ცოტა ქლორიდს.
წყლის სიხისტე. მითითებულია კალციუმის და მაგნიუმის მარილების ნაცვლად. წყალი დაყავით პატარა ნაჭრებად, თითო ნაჭრებად. შეგიძლიათ იხილოთ წყლის ბუნებრივი სიხისტე - ნაცრისფერი წყლის სიხისტე, სპეციფიკური სიხისტე, რომელიც იცვლება დუღილის ან დგომისას და არა გადასვლისას, რომელიც არ იკლებს წყლის ადუღების შემდეგ.
ბოსტნეული და ხორცი ცუდად იხარშება მყარ წყალში, რადგან მათში ნაპოვნი ცილები კალციუმთან და მაგნიუმთან ერთად ერწყმის არაორგანულ ნივთიერებებს, რომლებიც არ შეიწოვება ადამიანის ნაწლავებში.
ასეთი წყალი არ არის შესაფერისი ჰიგიენური პროცედურებისთვის: ის შეიცავს ჭარბი რაოდენობით მარილებს, რომლებიც გადმოედინება, არასასურველი ნარჩენები კი თმაზე დნება და მიტას წარმოქმნის.
სასმელი წყლის სიხისტე შეიძლება აღემატებოდეს 7 მგ/ლ. ეს მახასიათებელი შეიძლება გამოიხატოს გრადუსით (1 მგ/ეკვ წყლის სიხისტე უდრის 2,8 °). მყარი წყალი არის წყალი, რომელიც 20°-ზე მეტია, რბილი წყალი 10°-ზე ნაკლებია.
მარილები ასხამენ. წყალი, რომელიც ასხამს, არ არის იაფი, მაგრამ ზედმეტი რაოდენობით იგი ანიჭებს მწარე მეტალის გემოს და მოყვითალო ან მოყვითალო-ყავისფერ არომატს, ამცირებს გამჭვირვალობას. დასაშვებია სასმელი წყლის შემცველობა 0,5 მგ/ლ-მდე (ცივ წყალსატევებში) და 1,0 მგ/ლ-მდე (მიწისქვეშა წყლის ობიექტებში).
ფტორი. რაც არ უნდა იყოს სასმელ წყალში, ის მნიშვნელოვნად მიედინება კბილებზე. როდესაც კონცენტრაცია იზრდება, ხდება ფლუოროზი (კბილების მინანქარზე მუქი ლაქების გაჩენა), რაც იწვევს მათ შემდგომ გაფუჭებას, ხოლო კბილების არასაკმარისი გაფუჭების შემთხვევაში, კარიესის დაავადება ხშირდება. წყალი შეიცავს არაუმეტეს 1,5 მგ/ლ ფტორს, ოპტიმალური მჟავიანობაა 0,7-1,0 მგ/ლ. თუ ფტორი არ მოიხსნება, წყალი ინდივიდუალურად უნდა იყოს ფტორირებული და ნატრიუმის ფტორის დამატება.
წყლის ბუნებრივ (მიწიერ) სხეულებს აქვთ თვითგანწმენდის ბუნებრივი პროცესები, რადგან ადამიანებს არ შეუძლიათ მათი გადალახვა:
*უფასო ულტრაიისფერი გამოსხივებისგან;
*მნიშვნელოვანი ნაწილაკების დალექვა და გამოყოფა;
*ორგანული ნივთიერებების დაჟანგვა O2 შემცველობის გამო;
* ორგანული ჭარბი მინერალიზაცია ბაქტერიების ზრდის გამო.
მხარე 1
მდინარის წყლის შენახვა განისაზღვრება ნაკადების რაოდენობითა და სიძლიერით, რომლებიც მათში ჩაედინება მიწიდან და ქარიდან, აგრეთვე სამრეწველო და მუნიციპალური საწარმოების ჩამდინარე წყლებით.
მდინარის წყლის შენახვის კლასიფიკაცია ნაჩვენებია ნახ. 3.24 გამარტივებულია და ყოველთვის არ არის ეფექტური.
როგორც აჩვენა მდინარის წყლის შესანახი ფართომასშტაბიანი კვლევა, საცავის ავზიდან წყლის გამონადენის რეგულირება არ საჭიროებს იმდენ მნიშვნელოვან ცვლილებას, რამდენიც მდინარის წყლის განხორციელებაა შესაძლებელი. მიმდინარე მეთოდების გამოყენებითანალიზი.
სეზონური თავისებურებებიდან გამომდინარე, მდინარის წყლის საწყობში ცვლილებები უნდა აღდგეს მონტაჟის დაპროექტების დროს. მნიშვნელოვანი კათიონის კანის კლასი იყოფა სამ ჯგუფად: კალციუმი, მაგნიუმი და ნატრიუმი. თავისებურად, კანის ჯგუფი იყოფა წყლის ოთხ ტიპად, რომლებიც იდენტიფიცირებულია მრავალი იონით. კრემი შეიცავს მნიშვნელოვან კატიონებს, მდინარის წყალი შეიცავს იონებს K, NH4, Fe2, Mn2, Cu2, Zn2, Ni2, Fe3, Al3 და უფრო დაბალი კონცენტრაციით სხვა იონებს.
სიმძლავრის ცვლილებისა და მდინარის წყლის დინების ბუნების გასაგებად ნაფთა შემცველი წარმონაქმნების გასწვრივ, 1957 წ. TatNIPInafta-ს ბურღულებმა დამოუკიდებლად გაბურღეს ხუთი საინექციო საბურღი.
ახლომახლო დასახლებებიდა სამრეწველო ჩამდინარე წყლებს შეუძლიათ სამრეწველო ჩამდინარე წყლების დიდი ნაკადის მიწოდება მდინარის წყლის საწყობში.
მაგიდიდან ხელმძღვანელობით. 3 ფიგურა აჩვენებს, რომ მდინარის წყლის შენახვა განსხვავდება ფართო საზღვრებში. მდინარის წყლები, რომლებიც მიედინება ნაყოფიერ ადგილებში, სავსეა კარბონატებით და მაღალი კალციუმით. მდინარის წყლები, რომლებიც მიედინება მშრალ ადგილებში (მაგალითად, შეერთებული შტატების დასავლეთ ნაწილში) შეიცავს მეტ სულფატს, ნაკლებ კალციუმს და, შესაბამისად, ნაკლებ კარბონატს. არასწორი იქნება ორგანული სითხის რაოდენობის იგნორირება, რომელიც ტრანსპორტირდება წყლებით, რომლის ფრაგმენტები გარდაიქმნება ნაფტაში.
მიწისქვეშა წყლების ქიმიური შენახვა სანაპირო წყალმიმღებებში არის სხვა სიტყვებით რომ ვთქვათ, მდინარის წყლის შენახვა, რომელიც, თავისებურად, განიხილება როგორც ატმოსფერული ნალექების შესანახი, ასევე თოვლის, ქარიშხლისა და მიწისქვეშა ჩამონადენის შესანახი. ატმოსფეროში წვიმის წყალი და თოვლი გროვდება დიდი რაოდენობითმჟავიანობა, ნახშირორჟანგი, აზოტის ოქსიდი, ამონიუმის მარილები და ინდუსტრიული ტერიტორიების დაბინძურებულ გარემოში, როგორც ნივთიერება იგულისხმება, მათ ემატება ნახერხი, ბაქტერიები, სიროფი, ნახშირის წვის პროდუქტები, ნაფტა და სხვა ნივთიერებები.
შედეგად, მდინარის სიახლოვეს მიედინება მხოლოდ მცირე რაოდენობის შეფერხებული საკანალიზაციო წყალი, რის შედეგადაც ამოიწურება ჩამდინარე მდინარის წყლის საწყობი, რაც გამორიცხავს შემდგომი ლიკვიდაციის შესაძლებლობას.
სუნი კონცენტრირებულია მინერალების სახით, მაგალითად, თაბაშირი Ca8O4 - 2H2O, mirabilite Na28O4 - 10H2O და ასევე შედის ზღვის და მდინარის წყლის საწყობში.
ზემო მდინარის წყლები (ისევე, როგორც ტბები და წყლები) ხასიათდება მათი საცავების სიმრავლით, რაც გამოწვეულია წყალთან ახლოს მყოფი მცენარეებისა და არსებების ცხოვრებიდან და გაზაფხულის წყალდიდობის მთავარი მოვლენა და ფიცრები, რომლებიც იშლება. ნაპირებს ნიადაგის ნაწილაკების მნიშვნელოვან რაოდენობას. ამავდროულად, დასახლებულ პუნქტებთან ახლოს, ჩამდინარე წყლები და სამრეწველო საწარმოების ნარჩენები ხშირად ჩაედინება მდინარის წყლის საწყობში.
მდინარეში არსებული ქიმიური საწყობი ცნობს სეზონურ რყევებს. მდინარის წყლის ყველაზე დიდი მინერალიზაცია ხდება იმ პერიოდში, როდესაც მდინარე ცოცხალია მიწისქვეშა წყლებით და ყველაზე ნაკლებად გამოწვეულია წვიმების სეზონით ან ყინულის ფურცლების სიცოცხლის გამო. მდინარის წყლების შენახვა ფიზიკურ-გეოგრაფიული გონების ხელშია. მიწისზედა ზონებში წყლის მინერალიზაცია დაბალია. მინერალიზაცია ასევე იცვლება, როდესაც მდინარე მიედინება ჩამდინარე წყლებში, წყალმიმღები, რომელიც მდებარეობს სხვა ჩამოსხმის აუზებში.
მდინარის წყლის შენახვა, ისევე როგორც ნარჩენები, ინახება დროის ბოლომდე. ყველაზე ნაკლები ტალახიანობა და ყველაზე დიდი მინერალიზაცია ხდება ზამთარში, მაგრამ პირიქით ხდება წყალდიდობის დროს, განსაკუთრებით გაზაფხულზე. ბედის ჟამს მდინარის წყლის საწყობში მეტეოროლოგიური დრენაჟები, ზაფხულის ქარები და სხვა ფაქტორები ჩაედინება.
ბუნებრივი წყლების ქიმიური საწყობი ძალიან იშლება. მათ მეტი ოჯახი ჰყავთ ქიმიური ელემენტები, რომლებიც გამოითვლება გრამების ნაწილებად ან მთლიანი და თუნდაც ათობით ან ასობით გრამი ლიტრ წყალზე. ეს არის წყალში ნაპოვნი ელემენტები და იონების ან მოლეკულების გამოჩენა, რომლებიც ქმნიან რთულ სტრუქტურებს, მათ შორის ორგანულს.
წყლის მინერალიზაციის სტადიას და ბუნებას ამ და სხვა ადგილებში წყალი არღვევს. წყალში არამფრინავი მინერალური და ნაწილობრივ ორგანული ნივთიერებების დაშლის ადგილას ხასიათდება მშრალი ჭარბი რაოდენობა (ძირითადი რაოდენობა, ქლორიდების, სულფატების, კარბონატებისა და ბიკარბონატების მთლიანობა, მდელოს და მინდორ-მიწის ლითონები). წყლებმა, რომლებიც შეიცავს დიდი რაოდენობით მინერალურ მარილებს, შეიძლება მიანიჭონ უსიამოვნო მარილიანი ან მწარე-მარილიანი გემო, ამიტომ მშრალი ჭარბი სასმელი წყლის რაოდენობა ექვემდებარება სანიტარიულ პრაქტიკას მდინარეზე წყლის საზრიან სიმძლავრეზე შემოდინების გამო. თუნდაც 1000 მგ. /ლ. ექსპერიმენტულმა კვლევებმა აჩვენა, რომ ოპტიმალური (ორგანოლეფსიური თვისებები) არის მკვებავი წყალი, რომელიც შეიცავს 200-400 მგ მარილს ლიტრზე. 1000 მგ/ლ-მდე მშრალი ჭარბი წყალს უწოდებენ სუფთა, ხოლო 1000 მგ/ლ-ზე ზევით - მინერალიზებულს.
წყლის მინერალიზაციის პირველადი დონის ცვლილებები, თუ არა ბუნებრივი მიზეზების გამო (გაზაფხულის წყალდიდობა), შეიძლება ჩაითვალოს მესამე მხარის მდინარეების მიერ წყლის დაბინძურების მანიშნებლად.
წყალში ქლორიდები კონცენტრირებულია განსაკუთრებით ნატრიუმის ქლორიდის სახით და, სულ მცირე, სხვა ნაერთების (მაგნიუმის ქლორიდი და ა.შ.) სახით. ბუნებრივ წყლებში ქლორიდები ჩნდება ნიადაგის წარმონაქმნებიდან მათი მოცილების შედეგად. ქლორიდებით განსაკუთრებით მდიდარია მარილიანი ნიადაგის მქონე ადგილები. ქლორიდები მნიშვნელოვანია, როგორც ნივთიერებები, რომლებიც ცვლიან წყლის გემოს და გავლენას ახდენენ სხეულის ფიზიოლოგიურ ფუნქციებზე. 500 მგ/ლ კონცენტრაციიდან დაწყებული, ქლორიდები იწვევენ შლაკების სეკრეციის დათრგუნვას, რაც გამოიხატება მჟავიანობის და სიძლიერის ცვლილებაში შლაკების წვენის, რომელიც მომწამლავს. შედეგად, გემიდან სიცოცხლის ევაკუაცია დაჩქარდება. 1000 მგ/ლ-ზე მეტი კონცენტრაციით, ქლორიდი იწვევს დიურეზის ცვლილებას, რაც განსაკუთრებით საზიანოა იმ ადამიანებისთვის, რომლებსაც აწუხებთ გულის დაავადებები და ჯანმრთელობის პრობლემები. 350 მგ/ლ ქლორიდის ზემოთ კონცენტრაციისას ნარევს დაამატეთ მარილიანი წყალი.
ქლორიდები შეიძლება დაიკარგოს წყალში განავლით, კალმებიდან, სამზარეულოს ნარჩენებიდან, მუნიციპალური წყალმომარაგებისთვის, წყალი, რომელიც არ არის დაბინძურებული, ქლორიდები შეიძლება იყოს მნიშვნელოვანი, როგორც ყოველდღიური წყლის დაბინძურების არაპირდაპირი მაჩვენებელი. ვისში ქლორიდების კონცენტრაცია არ არის შეფასებული, რამდენია წყლის საათისა და მონაკვეთის ცვლილება, მაშინ. მატება საგანგებო, ბუნებრივი კონცენტრაციების წინააღმდეგ. ქლორიდების და ამიაკის ძლიერი არსებობა მცენარეებში მაღალი ჟანგვის და უსიამოვნო ბაქტერიოლოგიური მაჩვენებლების მქონე მცენარეებში მიუთითებს ამ წყლის სანიტარიულ პრობლემებზე.
სულფატები 500 მგ/ლ-ზე მეტი რაოდენობით, უმატებენ წყალს წყალში მარილიან ყლუპს, კონცენტრაციით 1000-1500 მგ/ლ და ზოგადად თრგუნავენ საფეთქლის სეკრეციას, აქვთ საფაღარათო მოქმედება ნაწლავებზე და იწვევს ნეგატიური დამოკიდებულება ადამიანების გემოვნებისადმი.მორწყავ იაკებს. სულფატები შეიძლება იყოს ზედაპირული წყლების დაბინძურების მაჩვენებელი ცხოველების ექსკრემენტებით, რადგან ცილის სხეულების შესანახი ნაწილია გოგირდი, რომელიც დაშლის და შემდგომი დაჟანგვისას გარდაიქმნება გოგირდმჟავას მარილში.
წყლის სიხისტე გვიჩვენებს მასში ორვალენტიანი ბალახის ლითონის კათიონების კონცენტრაციას, პირველ რიგში კალციუმის და მაგნიუმის. Ca(2+) და Мg(2+) იონები შეიძლება ასოცირებული იყოს სხვადასხვა ანიონებთან (HCO 3, SO 4, Cl, CO 3, HNO 3 და სხვ.).
კალციუმის და მაგნიუმის ჰიდროკარბონატები Ca(HCO 3) 2, Mg(HCO 3) 2 და კარბონატები CaCO 3, MgCO 3 მიუთითებს კარბონატის სიმტკიცეზე. წყლის გაცხელებისას კარბონატული ნარევი ნადგურდება (ცვლილება 2-მდე), რის შედეგადაც ჰიდროკარბონატები გადაიქცევა კარბონატებად.
კალციუმის და მაგნიუმის კარბონატებს შორის განსხვავება მნიშვნელოვნად ნაკლებია ჰიდროკარბონატებთან შედარებით, ამიტომ მდუღარე წყალთან ერთად სიხისტე მცირდება. წყლის სიხისტე, რომელიც შედგება კალციუმის და მაგნიუმის ჰიდროკარბონატებისგან, ეწოდება კარბონატს. კარბონატული სიხისტე ხშირად შერწყმულია ჩვეულებრივ სიმტკიცესთან, მაგრამ მათი სათითაოდ გათანაბრება შეუძლებელია. წყალში მაგნიუმის ჰიდროკარბონატის მაღალი კონცენტრაციით, განსხვავება კარბონატსა და ჩვეულებრივ სიმტკიცეს შორის შეიძლება იყოს მნიშვნელოვანი. შედარებითი სიხისტის ღირებულება პრაქტიკულად აცილებს წყლის ტენიანობას, რომელიც შეიცავს ნიადაგის ლითონების (Ca, Na, Mg, K) ჰიდროკარბონატების ნაცვლად და სუსტი მჟავების სხვა მარილებს. წყლის ტენიანობა მნიშვნელოვანია გაწმენდის დროს წყლის კოაგულაციის პროცესისთვის. განსხვავება სამართლებრივ და ჩვეულებრივ სისასტიკეს შორის ე.წ მუდმივი სისასტიკე, ის დაკავშირებულია დიდი რაოდენობით კალციუმთან და მაგნიუმთან, რომელიც დაკავშირებულია ჰიდროკარბონატების გარდა სხვა ანიონებთან (Cl, SO 4, NO 3 და ასე შემდეგ).
წყლის სიხისტე სასმელი წყლის სიხისტის ერთ-ერთი აუცილებელი კრიტერიუმია. მყარი წყალი არ არის შესაფერისი სახელმწიფო მიზნებისთვის: ბოსტნეული, ხორცი და ფრინველი იხარშება მყარ წყალში. გარეგანი სახეჩაის გემო და სიტკბო, ცუდია ტკბილად დალევა, ვინაიდან მასში ნატრიუმი წყალში კალციუმით და მაგნიუმით იცვლება, რის შედეგადაც წარმოიქმნება კალციუმის და მაგნიუმის შემცველობის ნალექი. მძიმე წყალმა შეიძლება გამოიწვიოს ავადმყოფობა და კანის სიმშრალე; ცხელი წყლით მომარაგების სისტემებში გათბობის მოწყობილობებში მყარი წყალი ქმნის მცირე ნალექს, რაც ართულებს მათ მუშაობას.
რაც შეეხება ჯანმრთელობას, მაღალი სიმწარე შეიძლება ჩაითვალოს ერთ-ერთ ფაქტორად, რომელიც ხელს უწყობს urolithiasis-ის განვითარებას, როგორც ზემოთ ითქვა. მომდევნო სამი საათის განმავლობაში განიხილება კვება, რათა გულ-სისხლძარღვთა სისტემაში სიხარბე შევიდეს; არსებობს მონაცემები გულის დაავადებით გამოწვეული სიკვდილიანობის შესახებ გამაგრილებელი წყლის მოხმარების გამო. ეს ჰიპოთეზა ბევრ ქვეყანაში არ არის დადასტურებული.
იგი ხვდება შექმნილი ორგანიზმის უხილავ ნაწილში და გამოიყენება დიქოლიური ფერმენტების (ჰემოგლობინი, კატალაზა და სხვ.) სტიმულირებისთვის. მისი დანახვა შესაძლებელია ორგანიზმიდან ნაწლავების გავლით. ორგანიზმი ოთახში თავის მოთხოვნილებებს ძირითადად გარემოთი ცხოვრებით აკმაყოფილებს, რამდენად დიდია ის სხეულში შესვლისას. წყლის დალევა, არ აქვს რეალური ფიზიოლოგიური მნიშვნელობა. Fe(2+), Fe(3+) გამოყოფა ხდება ყველა ბუნებრივ წყალში სხვადასხვა კონცენტრაციით. წყლის ობიექტებში მაღალი კონცენტრაციით, შედეგი არის ჩამდინარე წყლების შეგროვება. როდესაც წყალი ნაწილდება ფოლადის (არაგალავანზირებული) მილებით, მასში შესვლის ნაცვლად, კოროზია იზრდება. ორგანიზმზე მიღებისას ტოქსიკური ეფექტი უცნობია. პერორალურად მიღებისას უფრო დიდი დოზები (300 მგ/კგ ან მეტი) გამოიყენებოდა გასტროენტერიტის თავიდან ასაცილებლად ინტოქსიკაციის ნიშნების გარეშე. ამიტომ, წყლის მახლობლად ყოფნა არ არის გამოწვეული ესთეტიკური და ყოველდღიური გაღიზიანებით, ამიტომ წყალს ანიჭებს კალამუტნოსტს, მომზადებას და მწარე მეტალის გემოს. გარდა ამისა, წყალში მარილიანობის გაზრდილი კონცენტრაცია ხელს უწყობს სანერწყვე ბაქტერიების განვითარებას; როდესაც წყლის მილები კვდება, გროვდება მძიმე ნალექი, რაც ცვლის მათ დიამეტრს. დადგენილია, რომ წყლის გამჭვირვალობისა და ფერის მატება ხდება როგორც მჟავე, ისე ოქსიდური სითხეების შეყვანისას და ყველა შემთხვევაში სუნი გამოწვეულია სითხეში ჰიდროქსიდის არსებობით. როდესაც წყლის კონცენტრაცია იცვლება 0,3 მგ/ლ-მდე, წყლის გამჭვირვალობა და ფერი ტოლია სტანდარტისა. წყლის მეტალის გემო ჩნდება 0,5 მგ/ლ კონცენტრაციით. მოსახლეობასთან ექსპერიმენტების მეთოდიდან გამომდინარე, ცხადია, რომ საინფუზიო ტევადობის საგრძნობლად დიდი (1,0 მგ/ლ-ზე მეტი) წყალმა შეიძლება გამოიწვიოს სხვადასხვა ზემოქმედება ადამიანის კანზე, მათ შორის ქავილი და სიმშრალე.
წყლის ფერის საჭირო სტანდარტამდე მისასვლელად, წყლის გამწმენდ ნაგებობებში გამოიყენება წყლის ფერის შეღებვის სპეციალური მეთოდები. წყალში სულფატების, ქლორიდების და სხვა მარილების ჩანაცვლების მიზნით, წყლის დემარილირება ხდება სხვადასხვა მარილების დამატებით. დეზალიზაცია ხორციელდება დისტილაციის, იონური გაცვლის და ელექტროდიალიზის მეთოდების გამოყენებით. ადგილობრივი წყალმომარაგების გონებაში გამოიყენება ბუნებრივი სიცივით გაყინვის მეთოდი და ნაჭრის გაყინვა.
წყლის დეზინფექციისთვის გამოიყენება შემდეგი მეთოდები: აერაცია (დაჟანგვა) და შემდგომ ამოღებული სითხიდან ამოღებული ჰიდროქსიდით გაჟღენთვა დადგომით და ფილტრაციით: აგრეთვე წყლის ვიკორისტული კოაგულაცია და კატიონიზაცია.
წყლის დარბილების მიზნით (წყლის კათიონების Ca(2+) და Mg(2+) მუდმივი ან ნაწილობრივი მოცილება) გამოიყენება რეაგენტის მეთოდები, რომლებიც დაფუძნებულია წყლის დამუშავებაზე რეაგენტებით, რომლებიც აერთიანებს კალციუმის და მაგნიუმის იონებს, რომლებიც პრაქტიკულად შეუცვლელია ალყაში მოქცეული. (რისთვისაც საჭიროა სოდასთან შერწყმისას ჩამქრალი ორთქლის დამატება). უფრო პრაქტიკულიასევე მიღებულია იონგაცვლის მეთოდი იონგაცვლის ფისებიდან წყლის დარბილებისთვის. წყლის დარბილება იონგაცვლის მეთოდით შეიძლება განხორციელდეს N-კატიონური აბაზანების, H-კატიონური აბაზანების, პარალელური ან შემდგომი N-Na-კატიონური აბაზანების გამოყენებით.
წყლის სანიტარიულ-ქიმიურ ანალიზში მნიშვნელოვან როლს ასრულებს ამიაკის მარილების, აზოტისა და აზოტის მჟავების (ნიტრიტები და ნიტრატები) კონცენტრაცია, რაც ორგანული ნარჩენებით წყლის დაბინძურების არაპირდაპირი მაჩვენებელია.
შექმნილი ბუნების ორგანული ნივთიერებები, რომლებიც გვხვდება წყალში, ექვემდებარება დაშლას, ხოლო მინერალიზაცია ხდება წყალში ბინადრობს მიკროორგანიზმების არსებობის გამო. ეს პროცესი უფრო ინტენსიურად მიმდინარეობს თბილ ამინდში და წყალში მჟავას არსებობის გამო. აზოტის შემცველი ორგანული ნივთიერებების მინერალიზაცია ხდება ორ ფაზაში. პირველ ფაზაში, რომელსაც ამონიფიკაციას უწოდებენ, ცილები და ნივთიერებები იშლება ამინომჟავებად და მარილებად. ცილების დაშლა ხდება ანაერობების (B.putrificus, B.sporogenes და სხვ.), ფაკულტატური ანაერობების (B.micoides და სხვ.) და აერობების (B.mesentericus, B.subtilis და სხვა) შემოდინებით. თესლის ამონიფიკაცია გამოწვეულია ურობაქტერიებითა და მიკრობებით. ამიაკის ნარჩენები არის კობოს პროდუქტი, რომლის არსებობა საუბრობს სუფთა ორგანულ ფერმენტირებულ წყალზე.
მინერალიზაციის სხვა ფაზაში - ნიტრიფიკაცია - ამიაკი და მარილები იჟანგება ნიტრიტებად (B.nitrosomonas-ის დახმარებით), ხოლო სუნი იჟანგება ნიტრატებად (B.nitrobakter-ის დახმარებით). ამონიუმის მარილების ნიტრიტით აღდგენისთვის საჭიროა დაადასტუროთ, რომ წყალი ცოტა ხნის წინ დაბინძურდა ორგანული ნივთიერებებით. ნიტრატები ორგანული ნაერთების მინერალიზაციის ტერმინალური პროდუქტია და მათი არსებობა წყლის ხანგრძლივი მინარევების მაჩვენებელია.
აზოტის ნაერთები საშუალებას გვაძლევს დავადგინოთ წყლის დაბინძურების არსებობა და იქნება ინფორმაცია დაბინძურების ასაკის შესახებ. ამრიგად, თუ განმეორებითი ანალიზების დროს წყალში ამიაკის არსებობა აღარ გაიზარდა, შესაძლებელია დასკვნის გაკეთება, რომ წყალი დაბინძურდა და აღარ ბინძურდება. ამიაკის პარალელურად წყალში ჩნდება ნიტრიტები, რაც მიუთითებს, რომ ბოლო დროს სისტემატურად დაბინძურებული წყალია. და თუ წყალში არის ამიაკი, ნიტრიტები და ნიტრატები, მაშინ ეს მიუთითებს უკიდურესად არახელსაყრელ წყლის რეზერვუარზე, რაც ნიშნავს დიდი ხნის განმავლობაში არსებულ და სტაბილურად დაბინძურებული წყლის რეზერვუარს.
თუ წყალი ყოველდღიურად ავლენს ნიტრატებს, ამიაკს და ნიტრატებს, ეს იმაზე მეტყველებს, რომ ორგანული ნივთიერებების მინერალიზაციის პროცესები დასრულებულია და შესაბამისად, მინარევები მოიხსნება.
თუმცა უნდა აღინიშნოს, რომ წყლის ორგანული ნარჩენების ნაკადებით დაბინძურება არ არის წყალში აზოტის შემცველი ნაკადების გამოჩენის ერთადერთი მიზეზი. სუფთა წყლებში, რომლებიც ღრმად დევს, მჟავიანობა შეიძლება მოხდეს ყოველდღე, რის გამოც იქმნება სარეცხი საშუალებები ნიტრიტებისა და ამიაკის მინერალური ნარჩენების განახლებისთვის. მარილის ამიაკის და ნიტრიტების კონცენტრაციის ამ ტიპის მატება ღრმა ინტერსტრატულ წყლებში არ მიუთითებს ობსტრუქციაზე. წყლის შეფერხების სხვა ნიშნები გამოჩნდება მთელი დღის განმავლობაში.
წყალში გაჟღენთილ წყალში ამონიუმის მარილები, ნიტრიტები და ნიტრატები შეიძლება იყოს დაშლის პროდუქტები და წარმოადგენენ წყალში დეპონირების ორგანული ნივთიერებების დაშლის პროდუქტებს. აზოტის შემცველი ნივთიერებები შეიძლება დაიკარგოს წყალმომარაგებიდან სამრეწველო ჩამდინარე წყლებით, აგრეთვე ჩამდინარე წყლებიდან იმ ტერიტორიებიდან, რომლებიც აშკარად განაყოფიერებულია აზოტის შემცველი ნივთიერებებით.
ამრიგად, წყალში აზოტოვანი ნაერთების არსებობის სწორი ჰიგიენური შეფასებისთვის აუცილებელია წყალში მათი გამოჩენის მიზეზის დადგენა. წყალში ორგანული ნივთიერებების მინარევების შესახებ უფრო დადებითად შეიძლება ვისაუბროთ იმაზე, რომ წყალში მინერალური აზოტის შემცველი ნაერთების პარალელურად ჩნდება მინარევების სხვა მაჩვენებლები: ქიმიური (მაღალი დაჟანგვა) და მიკრობიოლოგიური (დაბალი რაოდენობა, მაღალი რაოდენობა). უ ონკანის წყალი, რომელიც შეიძლება იყოს დაუბინძურებელი, მნიშვნელობას კარგავს ამონიუმის მარილები და ნიტრიტები, როგორც წყალში ეპიდემიოლოგიური პრობლემების არაპირდაპირი მაჩვენებლები. პროტე, ონკანის წყალში, რომელიც არ არის დაბინძურებული ქლორით, ამონიუმის მარილების ნაცვლად კონცენტრაცია არ უნდა აღემატებოდეს 0,5 მგ/ლ-ს, რადგან ნაკლები აქტიური ნივთიერების - ქლორამინების დამატებით, ინფექციისთვის ქლორის ვიტრატი იზრდება 2-4-ჯერ.
ადგილობრივ წყალმომარაგებში, დადგენილი ჰიგიენური ნორმებიდან გამომდინარე, დასაშვებია ამონიუმის მარილის აზოტი 0,1 მგ/ლ-მდე, ნიტრიტის აზოტი – 0,002 მგ/ლ-მდე. მინერალური ან წყალმცენარეების აქტივობის შედეგად ისინი მნიშვნელოვანია, როგორც ობსტრუქციის მაჩვენებლები და დაშვებულია წყლის ნაცვლად გამოყენება.
დამოუკიდებელ ინტერესს წარმოადგენს ნიტრატების დაკარგვა, რომლებიც იწვევენ მეტემოგლობინემიას სუნის მაღალი კონცენტრაციით. ნაწლავებში ნიტრატის ამჟამინდელი თეორიის თანახმად, ადამიანები აგრძელებენ ნიტრატირებას ბაქტერიების შემოდინებით, რომლებიც ყოყმანობენ ახალში. ნიტრიტების დატენიანება ტარდება მეტემოგლობინის სტაბილიზებამდე. ამრიგად, დაავადება ემყარება მჟავე შიმშილის იმავე სტადიას, რომლის სიმპტომები პირველ რიგში ვლინდება ბავშვებში, განსაკუთრებით გულმკერდის არეში, რაც მნიშვნელოვანია ინდივიდუალური მომზადების შემთხვევაში (მშრალი რძის ნარევების განზავება წყალთან შესარევად). ან მოხმარებისას, წყლის ფასი პიტიას. ხანდაზმული ბავშვები და მოზარდები ნაკლებად მგრძნობიარენი არიან დაავადების მიმართ, რადგან მათ აქვთ კომპენსატორული მექანიზმების უფრო ძლიერი გამოხატულება. ნიტრატების კონცენტრაცია უდრის 45 მგ/ლ (NO 3-ად გარდაქმნისას) და უსაფრთხოდ მიიღება როგორც GDC სასმელ წყალში. ნიტრატების მაღალი კონცენტრაცია ძირითადად მიწისქვეშა წყლებშია, რაც წყლის მუდმივი ობსტრუქციის (განსაკუთრებით მიწისქვეშა წყლების) და მინერალური ცვლილებების მემკვიდრეობაა წყლის შემცველი ქანების გეოქიმიურ მახასიათებლებთან დაკავშირებით. წყლით გაჟღენთილ წყალში ნიტრატების კონცენტრაცია, როგორც წესი, არ არის მაღალი, დარჩენილი სურნელი კი წყლის ლინტს უკავშირდება. დამნაშავე შეიძლება იყოს მასიური დაბინძურება წყლით და ჩამდინარე წყლებით, რაც ხელს შეუშლის ნიტრატებს.
ნიტრიტები, როგორც არასტაბილური ნაერთები, არ გროვდება წყალში ტოქსიკური კონცენტრაციით, ამიტომ მათ არ აქვთ მნიშვნელობა, როგორც მეტემოგლობინის შემცველი ჰიდროქსიდი.
კბილის კარიესის ერთ-ერთი ყველაზე მნიშვნელოვანი მიზეზი არის სასმელ წყალში ფტორის ნაკლებობა და, შედეგად, ორგანიზმში ფტორის ნაკლებობა. უფრთხილდით სასმელ წყალში ფტორის პირდაპირ არსებობას და კბილის კარიესის რისკს. ფტორი კალციუმთან და ფოსფორთან ერთად უზრუნველყოფს ჯაგრისების და კბილების სიმტკიცეს და რბილობას.
ფტორს აქვს ჰემატოგენური ეფექტი გაჟღენთვის შემდეგ სცილიკოინტესტინალური ტრაქტი. ერთის მხრივ, ფტორი ასტიმულირებს კბილის მინერალიზაციის პროცესს, მეორეს მხრივ, რის შედეგადაც ხდება ფტორპატიტი, ცვლის კბილის მყარი ქსოვილების სტრუქტურას, რითაც ზრდის მათ წინააღმდეგობას ქიმიურ და ბიოლოგიურ კარიესოგენურ ფაქტორებზე, რომლებიც მოქმედებს პირი ცარიელი.
ზედაპირულ წყლებში ფტორის იონის კონცენტრაცია მნიშვნელოვანია 0,5 მგ/ლ-მდე და ამ წყლების წყალი ვიკორისტურია შუა და დიდი ადგილების უმეტესობისთვის. სასმელ წყალში ფტორის ოპტიმალური კონცენტრაცია არის 0,7-დან 1,2 მგ/ლ-მდე. ფტორის დაბალი კონცენტრაცია ზრდის კარიესის სიმძიმეს. ჭარბი ფტორი (1,5 მგ/ლ-ზე მეტი) იწვევს ფლუოროზს, რაც გავლენას ახდენს რეპროდუქციულ ჯანმრთელობაზე, განსაკუთრებით ბამბაზე. რესპირატორული დაავადებების სიხშირე და ფტორის მაღალი კონცენტრაცია საიმედოა.
როდესაც ფტორის შემცველობა 0,5 მგ/ლ-ზე დაბალია, რეკომენდებულია ონკანის წყლის ფტორიანი მიღება, რაც ამცირებს კბილის კარიესის სიხშირეს 65-70%-ით. უნდა გვახსოვდეს, რომ წყლიდან ფტორის შეწოვა 20%-ით უფრო სწრაფად ხდება, ვიდრე პროდუქტებიდან, რაც უზრუნველყოფს წყლის ფტორირებამდე ფრთხილად ინსტალაციას. წყლის ამჟამინდელი ფტორიდაციით, მისი ფტორიდის შემცველობა კანის კლიმატური რეგიონის დასაშვები მაქსიმალური დონის 70-80%-ს შორისაა. როდესაც ფტორი არის ზღვის დონიდან, წყალში შეიძლება მოხდეს დეფტორირება.
სასმელ წყალში ბუნებრივი წყლის შესანახად დამახასიათებელი ქიმიური ელემენტებისა და მარილების ნარევი შეიძლება შეიცავდეს არსებულ ქიმიკატებს და ნივთიერებებს, რომლებიც იკარგება სამრეწველო და სასოფლო-სამეურნეო წყლებში, აგრეთვე ჭარბი სითხე და ნაკადები, რომლებიც წყალს ემატება სინჯის აღებიდან ერთი საათის განმავლობაში. წყლის გამწმენდ ქარხნებში. მათთვის შეიქმნა GDK, როგორც ეს წარმოდგენილია SanPiN-ებში. ერთ-ერთი ასეთი ელემენტია ჭარბი აქტიური ქლორი, რომელსაც უმატებენ დაუბინძურებელ წყალს. არადაბინძურების ეფექტის მისაღწევად, ქლორის შემცველ პრეპარატებს ემატება მცირე რაოდენობით, ისე, რომ 30 წუთის შემდეგ წყალთან და ქლორთან შეხების შემდეგ (საკმარისია მიკროორგანიზმების ვეგეტატიური ფორმების შესამცირებლად), წყალში გარკვეული ჭარბი (). ჭარბი წყალში).0.3-დან 0.5მგ/ლ-მდე. დიდი რაოდენობით წყალს უსიამოვნო სუნი შემატებს, განსაკუთრებით წყალში ფენოლების არსებობისა და ჰალოგენირებული ნახშირწყლების არსებობის გამო, რაც შეიძლება იყოს კანცეროგენული.
| სტატისტიკა თემაზე: | |
|
ვირჩევთ ჟალუზებს აივნებისა და ლოჯიების ფანჯრებისთვის
ჟალუზები აივანზე არის ოპტიმალური გადაწყვეტა მშვიდი და ყოველდღიური საცხოვრებელი სივრცისთვის... არატურბო მარჯნის ფერი ინტერიერში ლურჯი და მარჯნის ინტეგრაცია ინტერიერში
და ერთ-ერთი ასეთი ფერი, საიდანაც შეგიძლიათ მიაღწიოთ დიდს... როდოდენდრონის დარგვა და მოვლა კანადური როდოდენდრონის დარგვა და მოვლა
უცხოურ ლიტერატურაში როდოდენდრონები მცენარეთა ჯგუფში მოჰყავთ გასაშენებლად. | |